Содержание
«Почему в носоглотке постоянно скапливается густая слизь?» — Яндекс Кью
Популярное
Сообщества
МедицинаЛор
Анонимный вопрос
·
98,4 K
Ответить1Уточнить
Зайцев Владимир Михайлович
Медицина
2,2 K
Главный врач ЛОР-клиники в Москве. Врач-оториноларинголог высшей категории. Кандидат… · 16 июл 2020 · dr-zaytsev.ru
Скопление слизи в глотке — состояние неприятное, но излечимое. Главное — точно определить причину этого симптома, и устранить её.
В медицине даже существует специальный термин, который употребляется при постоянно стекающей слизи в глотку из носовой полости — постназальный синдром. По сути, это тот же насморк, но наоборот.
Почему в носоглотке постоянно скапливается густая слизь?
- Причины постоянно скапливающейся слизи в глотке могут быть инфекционной и неинфекционной природы. К ним относят: Воспалительные заболевания носоглотки и гортани (синуситы, фарингит, ларингит). Усиленная выработка слизистого секрета в этот период связана с попыткой организма прочистить дыхательные пути от бактерий и вирусов, тем самым ускорив выздоровление. То, что слизь в этом случае выделяется обильно, наоборот, является вариантом нормы.
- Хронические заболевания верхних дыхательных путей. Эти заболевания вызывают воспалительные процессы в носоглотке, в результате чего здесь формируется постоянный источник инфекции.
- Заболевания нижних дыхательных путей (бронхит, воспаление лёгких, туберкулёз).
- Аллергические реакции на внешний раздражитель. Аллергия может сопровождаться обильным скоплением мокроты, которая мешает и её хочется постоянно сглатывать.
- Нарушения в работе желудочно-кишечного тракта, при которых содержимое желудка забрасывается обратно в пищевод и далее в глотку (гастроэзофагеальная рефлюксная болезнь, гастрит, язва).

- Особенности строения носовой полости (искривлённая носовая перегородка, увеличенные носовые раковины).
- Аденоиды.
- Неправильное питание — употребление слишком жирной или острой пищи раздражает органы ЖКТ и может спровоцировать усиленную выработку секрета.
- Вредные привычки. Табакокурение и злоупотребление алкогольными напитками приводит к ожогам слизистой оболочки глотки. Организм пытается избавиться от пагубного воздействия вредных веществ, усиленно вырабатывая слизистые массы.
- Попадание в носовую полость посторонних предметов.
- Плохая экологическая обстановка в месте проживания — загрязнённый воздух и пыль. Таким способом организм пытается избавиться от вредных частиц, попавших с воздухом.
Чтобы понять, как избавиться от слизи, нужно обратиться к лор-врачу для определения причины постназального синдрома.
Определением причины скопления слизистых масс занимается врач — оториноларинголог. Иногда приходится дополнительно обращаться к смежным специалистам: аллергологу, гастроэнтерологу и т. п. После установления причины неприятного состояния, пациенту будет назначена эффективная схема лечения, направленная не только на избавление от мокроты, но и на терапию основного заболевания.
п. После установления причины неприятного состояния, пациенту будет назначена эффективная схема лечения, направленная не только на избавление от мокроты, но и на терапию основного заболевания.
Как избавиться от слизи в глотке?
- Пациенту лор-врач обязательно порекомендует скорректировать количество употребляемой жидкости: необходимо пить больше тёплой жидкости, чтобы разжижить слизь (разумеется, если у больного нет проблем с почками).
- Больному назначают отхаркивающие препараты и лекарства для разжижения мокроты (муколитики), чтобы ускорить её отхождение.
- Если мокрота образуется из-за инфекционного заболевания, врач назначает антибактериальную либо противовирусную терапию (препарат, его дозировку и курс приёма также определяет оториноларинголог).
- Если причина в аллергии, назначаются антигистаминные препараты. Дальнейшим лечением занимается врач — аллерголог.
- При диагностировании проблем с ЖКТ необходимо пройти курс лечения у гастроэнтеролога.

- Местная терапия также включает использование антисептических спреев (например, «Мирамистин»), приём иммуностимуляторов («Имудон», «Лизобакт»). Отлично дополнят основное лечение и ускорят процесс выздоровления физиотерапевтические процедуры в лор-клинике.
Подробно о стекании слизи по носоглотке рассказываю в своей статье
Если у Вас остались вопросы по лор-тематике, или Вам нужна профессиональная помощь лор-врача, обращайтесь.
Я на связи!
Буду рад помочь!
Всегда Ваш, доктор Зайцев
ЛОР клиника доктора Зайцева
Москва, 5-й Монетчиковский пер, 14;
8(495) 642-45-25
Перейти на dr-zaytsev.ru
111,6 K
Луиза Шагаева
12 октября 2020
А можно узнать цену консультации у Вас?
Комментировать ответ…Комментировать…
Боклин Андрей Кузьмич
Медицина
5,4 K
Врач оториноларинголог хирург, кандидат медицинских наук Боклин Андрей Кузьмич. Врач… · 12 янв 2019 · boklin.ru
Врач… · 12 янв 2019 · boklin.ru
Это может быть как симптомом распространенных заболеваний: ринита, синусита, евстахиита. Так и менее часто встречающихся, например: назального полипоза (полип носа).
Необходим осмотр специалиста.
44,1 K
Комментировать ответ…Комментировать…
Вы знаете ответ на этот вопрос?
Поделитесь своим опытом и знаниями
Войти и ответить на вопрос
Как избавиться от слизи в дыхательных путях
Слизь в дыхательных путях, как правило, появляется в периоды межсезонья, когда увеличивается риск заболеть простудой и респираторными инфекциями. В это время иммунитет ослабевает, поэтому создаются оптимальные условия для развития патогенной микрофлоры в горле, носу, бронхах и легких. Появление слизи свидетельствует о развитии воспалительного процесса, поэтому от неё лучше поскорее избавляться.
Слизь или мокрота продуцируется бокаловидными секреторными клетками в дыхательных путях. Она в минимальных количествах есть всегда, потому что увлажняет реснитчатый эпителий, выстилающий отделы бронхиального дерева. Но когда в ней начинает развиваться патогенная микрофлора, то её становится больше. Так организм пытается эвакуировать болезнетворные агенты из горла. Но, как часто бывает, микробы развиваются быстрее. Тогда мокрота становится густой, забивает ворсинки, что замедляет выведение вязкого секрета. Получается, что образование слизи превышает скорость её удаления. Влажная и теплая среда — это отличное место для стремительного размножения бактерий. Так начинаются бронхиты, которые могут перейти в пневмонию.
Она в минимальных количествах есть всегда, потому что увлажняет реснитчатый эпителий, выстилающий отделы бронхиального дерева. Но когда в ней начинает развиваться патогенная микрофлора, то её становится больше. Так организм пытается эвакуировать болезнетворные агенты из горла. Но, как часто бывает, микробы развиваются быстрее. Тогда мокрота становится густой, забивает ворсинки, что замедляет выведение вязкого секрета. Получается, что образование слизи превышает скорость её удаления. Влажная и теплая среда — это отличное место для стремительного размножения бактерий. Так начинаются бронхиты, которые могут перейти в пневмонию.
Если причина выделения мокроты заключается в проникновении в дыхательные пути бактерий или раздражающих агентов, например, пыли или дыма, то нужно прокашляться. Это самый простой способ удаления мокроты. Однако при этом не следует делать чрезмерных усилий. Если мокрота не скашивается, а кашель давит и есть боль в груди, то это признаки воспалительного процесса. Как правило, клиника дополняется температурой, слабостью или лихорадкой. В таком случае лучше обратиться за помощью к врачу.
Как правило, клиника дополняется температурой, слабостью или лихорадкой. В таком случае лучше обратиться за помощью к врачу.
Можно также прополоскать горло. Для этого подойдет любое средство или даже теплая вода. Чаще всего используют раствор пищевой соды, соли или уксуса. В идеале нужно полоскать горло антисептическим раствором.
Медики постоянно советуют пить больше воды. Жидкость стимулирует выделение секрета и делает его не таким густым, поэтому мокрота лучше эвакуируется из дыхательных путей. При заболевании нужно пить теплую воду или чай с лимоном, настой шиповника, чай из смородины или малины, а также любые другие витаминизированные напитки.
Если не можете добиться разжижения мокроты, то нужно подышать парами пищевой соды. Она вступает в реакцию со слизью, разрушает химические связи между молекулами, что делает секрет более жидким. Приготовьте насыщенный содовый раствор, закипятите его. Снимите с плиты и вдыхайте пары, накрывшись полотенцем. Уже через несколько минут, если все сделали правильно, мокрота начнет отходить.
Важно следить за тем, чтобы воздух в помещении не был сухим, пыльным или затхлым. Для этого нужно проветривать, делать влажную уборку комнат и использовать увлажнитель. Нередко после устранения раздражителей, мокрота проходит сама.
Желательно отказаться от курения, потому что табачный дым сушит и обжигает слизистые оболочки дыхательных путей. Нежные ткани раздражаются и реагируют обильным выделением мокроты. Примерно то же происходит, когда человек вдыхает ядовитые пары, пыль или работает на вредном производстве. В таких случаях нужно использовать средства индивидуальной защиты или сменить сферу деятельности.
Можно попить отхаркивающие травы – отвары мать-и-мачехи, душицы, чабреца или алтея. Сироп корня солодки, подорожника или плюща — одни из самых эффективных натуральных средств от кашля и мокроты.
Кроме того, нужно больше двигаться. Когда человек подвержен гиподинамии, то от недостатка движения слизь не эвакуируется должным образом, поэтому скапливается в дыхательных путях. Сделайте простую, а лучше дыхательную гимнастику и сразу почувствуете облегчение.
Сделайте простую, а лучше дыхательную гимнастику и сразу почувствуете облегчение.
Если после указанных мер от слизи избавиться не удается, то нужно обратиться к врачу, — советуют на канале «Здоровье и Долголетие». Это нужно сделать немедленно, если заметили в слизи признаки крови или гнойных масс. Такие проявления могут говорить об очень сложных заболеваниях, которые требуют неотлагательной профессиональной терапии.
Что делать при заложенности носовых пазух и слизи — Справочник по здоровью носовых пазух
Вы чихаете, у вас болит горло и слизь течет из носа в течение всего дня; ты знаешь, что ты болен.
Но вы можете не знать, что вызывает ваши симптомы. Заложенность носовых пазух и чрезмерное выделение слизи возникают, когда ваше тело пытается защитить себя от чужеродных захватчиков или когда поражает инфекция.
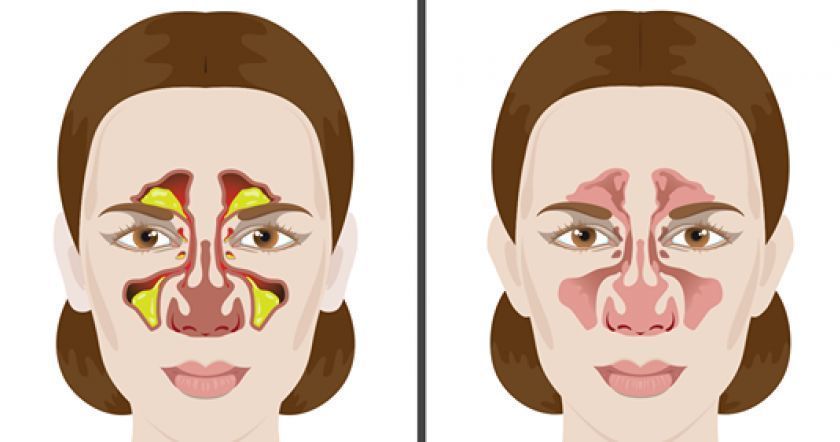
Называйте это как хотите, но то вещество, которое выходит из вашего носа, когда вы больны, — это слизь. Синусы, представляющие собой полые полости, заполненные воздухом, расположенные на лице, выстланы слизистой оболочкой.
Слизистые оболочки представляют собой тонкие слои влажных тканей, которые производят липкий материал, известный как слизь, которую вы выдыхаете из носа или откашливаете, когда у вас есть какое-либо заболевание. Он может быть прозрачным или желтым, имеет густую липкую консистенцию.
У слизи есть реальная цель. Он секретируется слизистыми оболочками для защиты дыхательных путей от крошечных захватчиков, таких как бактерии, вирусы, микробы и аллергены, которыми вы дышите. Слизь захватывает эти микробы, чтобы они не проникли глубже в дыхательные пути. Но иногда слизистые оболочки немного перебарщивают, что приводит к избыточному образованию слизи.
Что вызывает чрезмерное выделение слизи?
Заложенность носа или заложенность носа возникает, когда ткани, выстилающие носовые проходы, раздражаются, воспаляются и опухают, что затрудняет дыхание. Эти симптомы вызывает не слизь, забивающая нос, хотя раздражение носовых ходов может привести к чрезмерному выделению слизи. Заложенность носовых пазух возникает, когда слизистые оболочки раздражаются или инфицируются и начинают выделять больше слизи, чем обычно, заполняя эти полые области густой слизью.
Заложенность носовых пазух возникает, когда слизистые оболочки раздражаются или инфицируются и начинают выделять больше слизи, чем обычно, заполняя эти полые области густой слизью.
Все, что раздражает эти слизистые оболочки, может вызвать чрезмерное выделение слизи, включая следующие состояния здоровья:
- Бактериальная инфекция
- Вирусная инфекция (например, простуда или грипп)
- Аллергия (включая сенную лихорадку или чувствительность к пылевые клещи)
- Астма
- Предмет, застрявший в носу
- Синусовая инфекция
- Травма головы
- Чрезмерное использование назальных спреев другие симптомы тоже. Слизь может стекать в горло, например, вызывая кашель и боль в горле. Чрезмерная слизь также может скапливаться в ушах, закупоривая их, вызывая болезненность и иногда приводя к ушной инфекции.
Способы борьбы с обильным выделением слизи
Есть несколько способов избавиться от обильного выделения слизи и сопутствующих ему симптомов, таких как кашель и боль в горле.
 Если у вас есть бактериальная инфекция или аллергия, ваш врач может назначить лекарства, чтобы облегчить воспаление и отек, а также уменьшить выработку слизи.
Если у вас есть бактериальная инфекция или аллергия, ваш врач может назначить лекарства, чтобы облегчить воспаление и отек, а также уменьшить выработку слизи.В домашних условиях вы можете предпринять следующие шаги, чтобы разжижить слизь и уменьшить заложенность носовых пазух:
- Попробуйте использовать назальный спрей с физиологическим раствором (не лекарственный) несколько раз в день.
- Рассмотрите возможность использования нети-пота для промывания носовых пазух (убедитесь, что вы используете только стерильную, предварительно кипяченую и охлажденную или дистиллированную воду).
- Ежедневно пейте много воды и других жидкостей.
- Включите увлажнитель воздуха в вашем доме, чтобы воздух оставался влажным (обязательно следуйте инструкциям производителя по ежедневной очистке увлажнителя, чтобы он не стал источником проблем с носовыми пазухами).
- Попробуйте безрецептурный антигистаминный препарат.
Чрезмерное выделение слизи — это всего лишь способ вашего организма защитить себя и не допустить проникновения микробов в легкие, но результатом может быть серьезный дискомфорт, пока вы не очистите все это.
 Позаботьтесь о себе домашними средствами, чтобы разжижить густые выделения, и обратитесь к врачу, если ваши симптомы не улучшатся.
Позаботьтесь о себе домашними средствами, чтобы разжижить густые выделения, и обратитесь к врачу, если ваши симптомы не улучшатся.Что такое полипы в носу? Симптомы, причины, диагностика, лечение и профилактика
от Бекки Упхэм
Жизнь, амплифицированная: Карри Айткен. Глотание?
Если глотание затруднено, возможно, у вас дисфагия, и вам может потребоваться лечение, чтобы вы могли глотать без боли.
Джули Маркс
Когда боль в горле считается хронической?
Конечно, боль в горле может раздражать. Но когда боль в горле не утихает, это может быть признаком серьезной проблемы, которую вы должны были проверить…
Диана Родригес Вот некоторые возможные причины.
Если у взрослого человека идет носовое кровотечение без видимой причины, это может быть связано с приемом лекарств, состоянием здоровья или просто с сухим воздухом.

Дженнифер Дж. Браун, доктор философии
Как безопасно использовать нети-пот
У вас есть аллергия и проблемы с носовыми пазухами? Вот как может помочь нети-пот.
Женевьева Скарано
NeilMed NasaFlo Neti Pot Обзор
NeilMed NasaFlo Neti Pot может помочь вам предотвратить аллергию и проблемы с носовыми пазухами.
Женевьев Скарано
7 факторов, повышающих риск ушных инфекций
Диана Родригес
Дениз Манн
Функция и дисфункция слизи дыхательных путей
1. Thornton DJ, Sheehan JK. От муцинов к слизи: к более последовательному пониманию этого существенного барьера. Proc Am Thorac Soc. 2004; 1:54–61. [PubMed] [Google Scholar]
2. Knowles MR, Boucher RC. Очищение от слизи как первичный врожденный защитный механизм дыхательных путей млекопитающих. Джей Клин Инвест. 2002; 109: 571–577. [Бесплатная статья PMC] [PubMed] [Google Scholar]
3. Thornton DJ, Rousseau K, McGuckin MA. Структура и функция полимерных муцинов в слизи дыхательных путей. Annu Rev Physiol. 2008;70:459–486. [PubMed] [Google Scholar]
4. Rose MC, Voynow JA. Гены муцина дыхательных путей и гликопротеины муцина в норме и при патологии. Physiol Rev. 2006; 86: 245–278. [PubMed] [Google Scholar]
5. Конус Р.А. Барьерные свойства слизи. Adv Drug Deliv Rev. 2009; 61:75–85. [PubMed] [Google Scholar]
6. Hattrup CL, Gendler SJ. Структура и функция муцинов клеточной поверхности (привязанных).
 Annu Rev Physiol. 2008; 70: 431–457. [PubMed] [Google Scholar]
Annu Rev Physiol. 2008; 70: 431–457. [PubMed] [Google Scholar]7. Линден С.К., Саттон П., Карлссон Н.Г., Королик В., МакГакин М.А. Муцины в барьере слизистой оболочки для инфекции. Иммунол слизистых оболочек. 2008; 1: 183–19.7. [Бесплатная статья PMC] [PubMed] [Google Scholar]
8. Macklem PT, Proctor DF, Hogg JC. Стабильность периферических дыхательных путей. Респир Физиол. 1970; 8: 191–203. [PubMed] [Google Scholar]
9. Кесимер М., Махов А.М., Гриффит Дж.Д., Вердуго П., Шихан Дж.К. Распаковка гелеобразующего муцина: вид организации MUC5B после высвобождения гранул. Am J Physiol Lung Cell Mol Physiol. 2010;298:L15–L22. [Бесплатная статья PMC] [PubMed] [Google Scholar]
10. Kim S, Shim JJ, Burgel PR, et al. IL-13-индуцированная экспрессия секреторного белка клеток Clara в эпителии дыхательных путей: роль сигнального пути EGFR. Am J Physiol Lung Cell Mol Physiol. 2002; 283:L67–L75. [PubMed] [Академия Google]
11. Evans CM, Williams OW, Tuvim MJ, et al.
 Муцин продуцируется клетками Клара в проксимальных дыхательных путях мышей, зараженных антигеном. Am J Respir Cell Mol Biol. 2004; 31: 382–394. [PubMed] [Google Scholar]
Муцин продуцируется клетками Клара в проксимальных дыхательных путях мышей, зараженных антигеном. Am J Respir Cell Mol Biol. 2004; 31: 382–394. [PubMed] [Google Scholar]12. Reader JR, Tepper JS, Schelegle ES, et al. Патогенез метаплазии слизистых клеток в мышиной модели астмы. Ам Джей Патол. 2003; 162: 2069–2078. [Статья бесплатно PMC] [PubMed] [Google Scholar]
13. Hayashi T, Ishii A, Nakai S, Hasegawa K. Ультраструктура метаплазии бокаловидных клеток из клеток Клара при аллергическом астматическом воспалении дыхательных путей на мышиной модели астмы в виво. Арка Вирхова. 2004; 444: 66–73. [PubMed] [Академия Google]
14. Zhu Y, Ehre C, Abdullah LH, et al. Дефект базовой секреции Munc13-2 -/- указывает на источник олигомерных муцинов в дыхательных путях мышей. Дж. Физиол. 2008; 586:1977–1992. [Бесплатная статья PMC] [PubMed] [Google Scholar]
15. Kesimer M, Kirkham S, Pickles RJ, et al. Культура клеток трахеобронхиальной поверхности раздела воздух-жидкость: модель врожденной защиты слизистой оболочки верхних дыхательных путей? Am J Physiol Lung Cell Mol Physiol.
 2009; 296:L92–L100. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2009; 296:L92–L100. [Бесплатная статья PMC] [PubMed] [Google Scholar]16. Evans SE, Xu Y, Tuvim MJ, Dickey BF. Индуцируемая врожденная резистентность легочного эпителия к инфекции. Annu Rev Physiol. 2010;72:413–435. [Бесплатная статья PMC] [PubMed] [Google Scholar]
17. Wine JJ, Joo NS. Подслизистые железы и защита дыхательных путей. Proc Am Thorac Soc. 2004; 1:47–53. [PubMed] [Google Scholar]
18. Rogers CS, Abraham WM, Brogden KA, et al. Легкие свиньи как потенциальная модель муковисцидоза. Am J Physiol Lung Cell Mol Physiol. 2008; 295:L240–L263. [Бесплатная статья PMC] [PubMed] [Google Scholar]
19. Plopper CG, Heidsiek JG, Weir AJ, George JA, Hyde DM. Трахеобронхиальный эпителий у взрослых макак-резусов: количественное гистохимическое и ультраструктурное исследование. Ам Дж Анат. 1989; 184:31–40. [PubMed] [Google Scholar]
20. Hays SR, Fahy JV. Характеристика ремоделирования слизистых клеток при муковисцидозе: связь с нейтрофилами. Am J Respir Crit Care Med.
 2006; 174:1018–1024. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2006; 174:1018–1024. [Бесплатная статья PMC] [PubMed] [Google Scholar]21. Hogg JC. Патофизиология ограничения воздушного потока при хронической обструктивной болезни легких. Ланцет. 2004;364:709–721. [PubMed] [Google Scholar]
22. Lai SK, Wang YY, Wirtz D, Hanes J. Микро- и макрореология слизи. Adv Drug Deliv Rev. 2009; 61:86–100. [Бесплатная статья PMC] [PubMed] [Google Scholar]
23. Рубин Б.К. Слизь и муцины. Отоларингол Clin North Am. 2010;43:27–34. [PubMed] [Google Scholar]
24. Kirkham S, Sheehan JK, Knight D, Richardson PS, Thornton DJ. Неоднородность слизи дыхательных путей: вариации количества и гликоформ основных олигомерных муцинов MUC5AC и MUC5B. Биохим Дж. 2002; 361:537–546. [Бесплатная статья PMC] [PubMed] [Google Scholar]
25. Смарт ДД. Основы и основные механизмы мукоадгезии. Adv Drug Deliv Rev. 2005; 57: 1556–1568. [PubMed] [Google Scholar]
26. Имберти А., Варрот А. Распознавание микробами гликоконъюгатов поверхности клеток человека.
 Curr Opin Struct Biol. 2008; 18: 567–576. [PubMed] [Google Scholar]
Curr Opin Struct Biol. 2008; 18: 567–576. [PubMed] [Google Scholar]27. Tesfaigzi Y. Регуляция метаплазии слизистых клеток при бронхиальной астме. Курр Мол Мед. 2008; 8: 408–415. [PubMed] [Google Scholar]
28. Chen Y, Zhao YH, Di YP, Wu R. Характеристика экспрессии гена муцина 5B человека в эпителии дыхательных путей и геномного клона амино-концевой и 5′-фланкирующей области. Am J Respir Cell Mol Biol. 2001; 25: 542–553. [PubMed] [Академия Google]
29. Нгуен Л.П., Омолуаби О., Парра С. и соавт. Хроническое воздействие бета-блокаторов ослабляет воспаление и содержание муцина в мышиной модели астмы. Am J Respir Cell Mol Biol. 2008; 38: 256–262. [Бесплатная статья PMC] [PubMed] [Google Scholar]
30. Young HW, Williams OW, Chandra D, et al. Центральная роль экспрессии Muc5ac в слизистой метаплазии и ее регуляция консервативными 5′-элементами. Am J Respir Cell Mol Biol. 2007; 37: 273–290. [Бесплатная статья PMC] [PubMed] [Google Scholar]
31. Holtzman MJ, Byers DE, Benoit LA, et al.
 Иммунные пути перевода вирусной инфекции в хроническое заболевание дыхательных путей. Ад Иммунол. 2009; 102: 245–276. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Иммунные пути перевода вирусной инфекции в хроническое заболевание дыхательных путей. Ад Иммунол. 2009; 102: 245–276. [Бесплатная статья PMC] [PubMed] [Google Scholar]32. Lappalainen U, Whitsett JA, Wert SE, Tichelaar JW, Bry K. Интерлейкин-1бета вызывает воспаление легких, эмфизему и ремоделирование дыхательных путей в легких взрослых мышей. Am J Respir Cell Mol Biol. 2005; 32:311–318. [PubMed] [Google Scholar]
33. Казалино-Мацуда С.М., Монзон М.Е., Дэй А.Дж., Фортеза Р.М. Фрагменты гиалуронана/CD44 опосредуют индуцированную окислительным стрессом активацию MUC5B в эпителии дыхательных путей. Am J Respir Cell Mol Biol. 2009 г.;40:277–285. [Бесплатная статья PMC] [PubMed] [Google Scholar]
34. Zuhdi Alimam M, Piazza FM, Selby DM, Letwin N, Huang L, Rose MC. Экспрессия матричной РНК и белка муцина Muc-5/5ac является маркером метаплазии бокаловидных клеток в дыхательных путях мышей. Am J Respir Cell Mol Biol. 2000; 22: 253–260. [PubMed] [Google Scholar]
35.
 Woodruff PG, Modrek B, Choy DF, et al. Воспаление, вызываемое Т-хелперами 2 типа, определяет основные субфенотипы астмы. Am J Respir Crit Care Med. 2009; 180:388–395. [Ошибка, Am J Respir Crit Care Med 2009; 180:796.] [Бесплатная статья PMC] [PubMed] [Google Scholar]
Woodruff PG, Modrek B, Choy DF, et al. Воспаление, вызываемое Т-хелперами 2 типа, определяет основные субфенотипы астмы. Am J Respir Crit Care Med. 2009; 180:388–395. [Ошибка, Am J Respir Crit Care Med 2009; 180:796.] [Бесплатная статья PMC] [PubMed] [Google Scholar]36. Zhen G, Park SW, Nguyenvu LT, et al. IL-13 и рецептор эпидермального фактора роста играют важную, но различную роль в продукции муцина эпителиальными клетками. Am J Respir Cell Mol Biol. 2007; 36: 244–253. [Бесплатная статья PMC] [PubMed] [Google Scholar]
37. Woodruff PG, Boushey HA, Dolganov GM, et al. Полногеномное профилирование идентифицирует гены эпителиальных клеток, связанные с астмой и реакцией на лечение кортикостероидами. Proc Natl Acad Sci U S A. 2007;104:15858–15863. [Бесплатная статья PMC] [PubMed] [Google Scholar]
38. Innes AL, Woodruff PG, Ferrando RE, et al. У курильщиков с обструкцией дыхательных путей увеличены запасы эпителиального муцина в крупных дыхательных путях. Грудь.
 2006; 130:1102–1108. [PubMed] [Google Scholar]
2006; 130:1102–1108. [PubMed] [Google Scholar]39. Chen G, Korfhagen TR, Xu Y, et al. SPDEF необходим для дифференцировки легочных бокаловидных клеток мышей и регулирует сеть генов, связанных с продукцией слизи. Джей Клин Инвест. 2009;119:2914–2924. [Бесплатная статья PMC] [PubMed] [Google Scholar]
40. Deshmukh HS, Shaver C, Case LM, et al. Акролеин-активируемая матриксная металлопротеиназа 9способствует постоянной выработке муцина. Am J Respir Cell Mol Biol. 2008; 38: 446–454. [Бесплатная статья PMC] [PubMed] [Google Scholar]
41. Takeyama K, Jung B, Shim JJ, et al. Активация рецепторов эпидермального фактора роста отвечает за синтез муцина, индуцированный сигаретным дымом. Am J Physiol Lung Cell Mol Physiol. 2001; 280:L165–L172. [PubMed] [Google Scholar]
42. Kettle R, Simmons J, Schindler F, et al. Регуляция индуцированной нейрегулином 1бета1 экспрессии MUC5AC и MUC5B в эпителии дыхательных путей человека. Am J Respir Cell Mol Biol. 2010;42:472–481.
 [PubMed] [Академия Google]
[PubMed] [Академия Google]43. Kuperman DA, Huang X, Koth LL, et al. Прямое воздействие интерлейкина-13 на эпителиальные клетки вызывает гиперреактивность дыхательных путей и гиперпродукцию слизи при астме. Нат Мед. 2002; 8: 885–889. [PubMed] [Google Scholar]
44. Куперман Д.А., Хуанг Х., Нгуенву Л., Хёльшер С., Бромбахер Ф., Эрле Д.Дж. Передача сигналов рецептора IL-4 в клетках Клара необходима для индуцированного аллергеном образования слизи. Дж Иммунол. 2005; 175:3746–3752. [PubMed] [Google Scholar]
45. Wan H, Kaestner KH, Ang SL, et al. Foxa2 регулирует альвеоляризацию и гиперплазию бокаловидных клеток. Разработка. 2004;131:953–964. [PubMed] [Google Scholar]
46. Burgel PR, Nadel JA. Врожденные иммунные реакции, опосредованные рецепторами эпидермального фактора роста, и их роль в заболеваниях дыхательных путей. Eur Respir J. 2008; 32: 1068–1081. [PubMed] [Google Scholar]
47. Друин С.М., Корри Д.Б., Холлман Т.Дж., Кильдсгаард Дж., Ветсель Р.
 А. Отсутствие комплементарного рецептора анафилатоксина C3a подавляет эффекторные функции Th3 в мышиной модели легочной аллергии. Дж Иммунол. 2002; 169: 5926–5933. [PubMed] [Google Scholar]
А. Отсутствие комплементарного рецептора анафилатоксина C3a подавляет эффекторные функции Th3 в мышиной модели легочной аллергии. Дж Иммунол. 2002; 169: 5926–5933. [PubMed] [Google Scholar]48. Humbles AA, Lu B, Nilsson CA, et al. Роль рецептора анафилатоксина C3a в эффекторной фазе астмы. Природа. 2000;406:998–1001. [PubMed] [Google Scholar]
49. Nguyen LP, Lin R, Parra S, et al. Передача сигналов бета2-адренорецепторов необходима для развития фенотипа астмы в мышиной модели. Proc Natl Acad Sci U S A. 2009;106:2435–2440. [Бесплатная статья PMC] [PubMed] [Google Scholar]
50. Davis CW, Dickey BF. Регулируемая секреция муцина бокаловидными клетками дыхательных путей. Annu Rev Physiol. 2008; 70: 487–512. [PubMed] [Google Scholar]
51. Tuvim MJ, Mospan AR, Burns KA, et al. Synaptotagmin 2 связывает экзоцитоз муциновых гранул с передачей сигналов Ca2+ от эндоплазматического ретикулума. Дж. Биол. Хим. 2009 г.;284:9781–9787. [Бесплатная статья PMC] [PubMed] [Google Scholar]
52.
 Curran DR, Cohn L. Успехи в метаплазии слизистых клеток: пробка для слизи как терапевтический фокус при хроническом заболевании дыхательных путей. Am J Respir Cell Mol Biol. 2010; 42: 268–275. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Curran DR, Cohn L. Успехи в метаплазии слизистых клеток: пробка для слизи как терапевтический фокус при хроническом заболевании дыхательных путей. Am J Respir Cell Mol Biol. 2010; 42: 268–275. [Бесплатная статья PMC] [PubMed] [Google Scholar]53. Peng J, Yang XO, Chang SH, Yang J, Dong C. Передача сигналов IL-23 усиливает поляризацию Th3 и регулирует аллергическое воспаление дыхательных путей. Сотовый рез. 2010;20:62–71. [Бесплатная статья PMC] [PubMed] [Google Scholar]
54. Хун Л.Я., Величко С., Хуанг Ф., Тай П., Ву Р. Регуляция врожденных и адаптивных иммунных реакций дыхательных путей: парадигма IL-17. Критический преподобный Иммунол. 2008; 28: 269–279. [PubMed] [Google Scholar]
55. Moghaddam SJ, Clement CG, De la Garza MM, et al. Лизат Haemophilus influenzae индуцирует аспекты фенотипа хронической обструктивной болезни легких. Am J Respir Cell Mol Biol. 2008; 38: 629–638. [Бесплатная статья PMC] [PubMed] [Google Scholar]
56. Neveu WA, Allard JB, Dienz O, et al.
 IL-6 необходим для образования слизи в дыхательных путях, вызванной вдыхаемыми грибковыми аллергенами. Дж Иммунол. 2009 г.;183:1732–1738. [Бесплатная статья PMC] [PubMed] [Google Scholar]
IL-6 необходим для образования слизи в дыхательных путях, вызванной вдыхаемыми грибковыми аллергенами. Дж Иммунол. 2009 г.;183:1732–1738. [Бесплатная статья PMC] [PubMed] [Google Scholar]57. Тай П., Лукоянов А., Вачи С., Ву Р. Регуляция экспрессии гена муцина дыхательных путей. Annu Rev Physiol. 2008; 70: 405–429. [Бесплатная статья PMC] [PubMed] [Google Scholar]
58. Adler KB, Li Y. Эпителий дыхательных путей и слизь: внутриклеточные сигнальные пути для экспрессии и секреции генов. Am J Respir Cell Mol Biol. 2001; 25: 397–400. [PubMed] [Google Scholar]
59. Kim KC, Hisatsune A, Kim DJ, Miyata T. Фармакология высвобождения муцина бокаловидными клетками дыхательных путей. J Pharmacol Sci. 2003;92: 301–307. [PubMed] [Google Scholar]
60. Lazarowski ER, Boucher RC. Пуринергические рецепторы в эпителии дыхательных путей. Курр Опин Фармакол. 2009; 9: 262–267. [Бесплатная статья PMC] [PubMed] [Google Scholar]
61. Davis CW, Lazarowski E. Связь активности ресничек дыхательных путей и секреции муцина с механическими стрессами посредством пуринергической передачи сигналов.
 Респир Физиол Нейробиол. 2008; 163: 208–213. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Респир Физиол Нейробиол. 2008; 163: 208–213. [Бесплатная статья PMC] [PubMed] [Google Scholar]62. Bateman ED, Rennard S, Barnes PJ, et al. Альтернативные механизмы для тиотропия. Пульм Фармакол Тер. 2009 г.;22:533–542. [PubMed] [Google Scholar]
63. Tarran R, Button B, Boucher RC. Регуляция нормального и муковисцидозного поверхностного объема жидкости в дыхательных путях с помощью фазового напряжения сдвига. Annu Rev Physiol. 2006; 68: 543–561. [PubMed] [Google Scholar]
64. Kummer W, Lips KS, Pfeil U. Эпителиальная холинергическая система дыхательных путей. Гистохим клеточной биологии. 2008; 130: 219–234. [Бесплатная статья PMC] [PubMed] [Google Scholar]
65. Hogg JC. Патология бронхиальной астмы. АПМИС. 1997; 105: 735–745. [PubMed] [Академия Google]
66. Hays SR, Fahy JV. Роль слизи в фатальной астме. Am J Med. 2003; 115: 68–69. [PubMed] [Google Scholar]
67. Bossé Y, Riesenfeld EP, Paré PD, Irvin CG. Это не все гладкие мышцы: негладкомышечные элементы контролируют сопротивление воздушному потоку.
 Annu Rev Physiol. 2010;72:437–462. [PubMed] [Google Scholar]
Annu Rev Physiol. 2010;72:437–462. [PubMed] [Google Scholar]68. Verdugo P. Секреция бокаловидных клеток и мукогенез. Annu Rev Physiol. 1990; 52: 157–176. [PubMed] [Google Scholar]
69. Boucher RC. Муковисцидоз: заболевание уязвимости к обезвоживанию поверхности дыхательных путей. Тренды Мол Мед. 2007; 13: 231–240. [PubMed] [Академия Google]
70. Ransford GA, Fregien N, Qiu F, Dahl G, Conner GE, Salathe M. Паннексин 1 способствует высвобождению АТФ в эпителии дыхательных путей. Am J Respir Cell Mol Biol. 2009; 41: 525–534. [Бесплатная статья PMC] [PubMed] [Google Scholar]
71. Kim KC, Lillehoj EP. Муцин MUC1: миротворец в легких. Am J Respir Cell Mol Biol. 2008; 39: 644–647. [PMC free article] [PubMed] [Google Scholar]
72. Davies JR, Kirkham S, Svitacheva N, Thornton DJ, Carlstedt I. MUC16 вырабатывается в поверхностном эпителии трахеи и подслизистых железах и присутствует в выделениях из нормальных дыхательных путей человека. и культивированные бронхиальные эпителиальные клетки.
 Int J Biochem Cell Biol. 2007;39: 1943–1954. [PubMed] [Google Scholar]
Int J Biochem Cell Biol. 2007;39: 1943–1954. [PubMed] [Google Scholar]73. Salathe M. Регуляция биения ресничек млекопитающих. Annu Rev Physiol. 2007; 69: 401–422. [PubMed] [Google Scholar]
74. Shah AS, Ben-Shahar Y, Moninger TO, Kline JN, Welsh MJ. Подвижные реснички эпителия дыхательных путей человека являются хемосенсорными. Наука. 2009; 325:1131–1134. [Бесплатная статья PMC] [PubMed] [Google Scholar]
75. Canning BJ. Анатомия и нейрофизиология кашлевого рефлекса: рекомендации ACCP по клинической практике, основанные на фактических данных. Грудь. 2006;129(Прил.): 33S–47S. [PubMed] [Google Scholar]
76. Рубин Б.К. Роль слизи в исследовании кашля. Легкое. 2010; 188 (Приложение): S69–S72. [PubMed] [Google Scholar]
77. Martinez S, Heyneman LE, McAdams HP, Rossi SE, Restrepo CS, Eraso A. Мукоидные сдавления: симптом пальца в перчатке и другие признаки КТ и рентгенографии. Рентгенография. 2008; 28:1369–1382. [PubMed] [Google Scholar]
78.
 Роу С.М., Миллер С., Соршер Э.Дж. Муковисцидоз. N Engl J Med. 2005; 352:1992–2001. [PubMed] [Академия Google]
Роу С.М., Миллер С., Соршер Э.Дж. Муковисцидоз. N Engl J Med. 2005; 352:1992–2001. [PubMed] [Академия Google]79. Дэвис П.Б. Муковисцидоз с 1938 года. Am J Respir Crit Care Med. 2006; 173: 475–482. [PubMed] [Google Scholar]
80. Chen EY, Yang N, Quinton PM, Chin WC. Новая роль бикарбоната в образовании слизи. Am J Physiol Lung Cell Mol Physiol. 2010;299:L542–L549. [Бесплатная статья PMC] [PubMed] [Google Scholar]
81. Mall M, Grubb BR, Harkema JR, O’Neal WK, Boucher RC. Повышенное поглощение Na+ эпителием дыхательных путей вызывает у мышей болезнь легких, подобную муковисцидозу. Нат Мед. 2004; 10: 487–49.3. [PubMed] [Google Scholar]
82. Поттер Дж.Л., Спектор С., Мэтьюз Л.В., Лемм Дж. Исследования легочных выделений. 3. Нуклеиновые кислоты в цельных легочных выделениях больных муковисцидозом, бронхоэктазами и ларингэктомией. Ам преподобный Респир Дис. 1969; 99: 909–916. [PubMed] [Google Scholar]
83. Vasconcellos CA, Allen PG, Wohl ME, Drazen JM, Janmey PA, Stossel TP.
 Уменьшение вязкости муковисцидозной мокроты in vitro гельсолином. Наука. 1994; 263:969–971. [PubMed] [Академия Google]
Уменьшение вязкости муковисцидозной мокроты in vitro гельсолином. Наука. 1994; 263:969–971. [PubMed] [Академия Google]84. Fahy JV, Kim KW, Liu J, Boushey HA. Выраженное нейтрофильное воспаление в мокроте у субъектов с обострением астмы. J Аллергия Клин Иммунол. 1995; 95: 843–852. [PubMed] [Google Scholar]
85. Отчет экспертной группы 3: рекомендации по диагностике и лечению астмы. Bethesda, MD: Национальный институт сердца, легких и крови; 2007. (http://www.nhlbi.nih.gov/guidelines/asthma.) [Google Scholar]
86. Bergeron C, Al-Ramli W, Hamid Q. Ремоделирование при астме. Proc Am Thorac Soc. 2009 г.;6:301–305. [PubMed] [Google Scholar]
87. Moro K, Yamada T, Tanabe M, et al. Врожденная продукция цитокинов T(H)2 лимфоидными клетками c-Kit(+)Sca-1(+), ассоциированными с жировой тканью. Природа. 2010; 463: 540–544. [PubMed] [Google Scholar]
88. Sheehan JK, Richardson PS, Fung DC, Howard M, Thornton DJ. Анализ гликопротеинов респираторной слизи при астме: подробное исследование пациента, умершего от астматического статуса.
 Am J Respir Cell Mol Biol. 1995; 13: 748–756. [PubMed] [Академия Google]
Am J Respir Cell Mol Biol. 1995; 13: 748–756. [PubMed] [Академия Google]89. Innes AL, Carrington SD, Thornton DJ, et al. Анализ мокроты ex vivo выявляет нарушение протеазозависимой деградации слизи белками плазмы при острой астме. Am J Respir Crit Care Med. 2009; 180: 203–210. [Бесплатная статья PMC] [PubMed] [Google Scholar]
90. Ordoñez CL, Shaughnessy TE, Matthay MA, Fahy JV. Увеличение числа нейтрофилов и уровня IL-8 в секрете дыхательных путей при острой тяжелой астме: клиническое и биологическое значение. Am J Respir Crit Care Med. 2000; 161:1185–119.0. [PubMed] [Google Scholar]
91. Siroux V, Boudier A, Bousquet J, et al. Фенотипические детерминанты неконтролируемой бронхиальной астмы. J Аллергия Клин Иммунол. 2009; 124: 681–687. [PubMed] [Google Scholar]
92. Hogg JC, Chu F, Utokaparch S, et al. Характер обструкции мелких дыхательных путей при хронической обструктивной болезни легких. N Engl J Med. 2004; 350:2645–2653. [PubMed] [Google Scholar]
93.
 Глобальная инициатива по хронической обструктивной болезни легких. обновления 2009 года. (http://www.goldcopd.com.) [Google Scholar]
Глобальная инициатива по хронической обструктивной болезни легких. обновления 2009 года. (http://www.goldcopd.com.) [Google Scholar]94. Леопольд П.Л., О’Махони М.Дж., Лиан К.Дж., Тилли А.Е., Харви Б.Г., Кристал Р.Г. Курение связано с укорочением ресничек дыхательных путей. ПЛОС ОДИН. 2009;4(12):e8157. [Бесплатная статья PMC] [PubMed] [Google Scholar]
95. Tamashiro E, Xiong G, Anselmo-Lima WT, Kreindler JL, Palmer JN, Cohen NA. Воздействие сигаретного дыма нарушает цилиогенез респираторного эпителия. Am J Rhinol Аллергия. 2009; 23:117–122. [PubMed] [Google Scholar]
96. Verra F, Escudier E, Lebargy F, Bernudin JF, De Crémoux H, Bignon J. Ресничные аномалии в бронхиальном эпителии курильщиков, бывших курильщиков и некурящих. Am J Respir Crit Care Med. 1995;151:630–634. [PubMed] [Google Scholar]
97. Cantin AM, Hanrahan JW, Bilodeau G, et al. Функция регулятора трансмембранной проводимости при муковисцидозе подавлена у курильщиков сигарет. Am J Respir Crit Care Med.
 2006; 173:1139–1144. [PubMed] [Google Scholar]
2006; 173:1139–1144. [PubMed] [Google Scholar]98. Sethi S, Murphy TF. Инфекция в патогенезе и течении хронической обструктивной болезни легких. N Engl J Med. 2008; 359: 2355–2365. [PubMed] [Google Scholar]
99. Совместное исследование генетики астмы (CSGA) Полногеномный поиск локусов предрасположенности к астме в этнически различных популяциях. Нат Жене. 1997;15:389–392. [PubMed] [Google Scholar]
100. Kamio K, Matsushita I, Hijikata M, et al. Анализ промотора и аберрантная экспрессия гена MUC5B при диффузном панбронхиолите. Am J Respir Crit Care Med. 2005; 171:949–957. [PubMed] [Google Scholar]
101. Flume PA, O’Sullivan BP, Robinson KA, et al. Легочные рекомендации по муковисцидозу: хронические лекарства для поддержания здоровья легких. Am J Respir Crit Care Med. 2007; 176: 957–969. [PubMed] [Google Scholar]
102. Flume PA, Mogayzel PJ, Jr, Robinson KA, et al. Руководство по муковисцидозу легких: лечение обострений легких. Am J Respir Crit Care Med.
 2009 г.;180:802–808. [PubMed] [Google Scholar]
2009 г.;180:802–808. [PubMed] [Google Scholar]103. Flume PA, Robinson KA, O’Sullivan BP, et al. Руководство по муковисцидозу легких: терапия очистки дыхательных путей. Уход за дыханием. 2009; 54: 522–537. [PubMed] [Google Scholar]
104. Boogaard R, de Jongste JC, Merkus PJ. Фармакотерапия нарушенного мукоцилиарного клиренса при заболеваниях легких у детей без муковисцидоза: обзор литературы. Педиатр Пульмонол. 2007; 42: 989–1001. [PubMed] [Google Scholar]
105. Роджерс Д.Ф. Мукоактивные средства при гиперсекреторных заболеваниях дыхательных путей. Уход за дыханием. 2007; 52: 1176–119.3. [PubMed] [Google Scholar]
106. Саутам Д.С., Эллис Р., Уотти Дж., Гласс В., Инман М.Д. Отскок бокаловидных клеток и дисфункция дыхательных путей при отмене кортикостероидов в мышиной модели астмы. Am J Respir Crit Care Med. 2008; 178:1115–1122. [PubMed] [Google Scholar]
107. Капур Н., Белл С., Колбе Дж., Чанг А.Б. Ингаляционные стероиды при бронхоэктазах. Кокрановская система базы данных, ред.
 2009; 1:CD000996. [PubMed] [Google Scholar]
2009; 1:CD000996. [PubMed] [Google Scholar]108. Woodruff PG, Wolff M, Hohlfeld JM, et al. Безопасность и эффективность ингаляционного ингибитора рецептора эпидермального фактора роста (BIBW 29).48 БС) при хронической обструктивной болезни легких. Am J Respir Crit Care Med. 2010; 181:438–445. [PubMed] [Google Scholar]
109. Сингер М., Мартин Л.Д., Варгафтиг Б.Б. и др. Родственный MARCKS пептид блокирует гиперсекрецию слизи в мышиной модели астмы. Нат Мед. 2004; 10: 193–196. [PubMed] [Google Scholar]
110. Chen S, Barbieri JT. Разработка ботулинического нейротоксина для расширения терапевтического вмешательства. Proc Natl Acad Sci U S A. 2009;106:9180–9184. [Бесплатная статья PMC] [PubMed] [Google Scholar]
111. Foster KA, Adams EJ, Durose L, et al. Реинжиниринг целевой специфичности клостридиальных нейротоксинов — путь к новым терапевтическим средствам. Нейротокс Рез. 2006; 9: 101–107. [PubMed] [Google Scholar]
112. Fahy JV, Steiger DJ, Liu J, Basbaum CB, Finkbeiner WE, Boushey HA.
 Маркеры секреции слизи и уровни ДНК в индуцированной мокроте больных астмой и здоровых людей. Ам преподобный Респир Дис. 1993; 147:1132–1137. [PubMed] [Google Scholar]
Маркеры секреции слизи и уровни ДНК в индуцированной мокроте больных астмой и здоровых людей. Ам преподобный Респир Дис. 1993; 147:1132–1137. [PubMed] [Google Scholar]113. О’Доннелл А.Е., Баркер А.Ф., Иловите Дж.С., Фик Р.Б. Лечение идиопатических бронхоэктазов аэрозольной рекомбинантной человеческой ДНКазой I. Грудь. 1998;113:1329–1334. [PubMed] [Google Scholar]
114. Дональдсон С.Х., Беннетт В.Д., Земан К.Л., Ноулз М.Р., Тарран Р., Буше Р.С. Клиренс слизи и функция легких при муковисцидозе с гипертоническим раствором. N Engl J Med. 2006; 354: 241–250. [PubMed] [Google Scholar]
115. Elkins MR, Robinson M, Rose BR, et al. Контролируемое исследование длительной ингаляции гипертонического солевого раствора у пациентов с муковисцидозом. N Engl J Med. 2006; 354: 229–240. [PubMed] [Google Scholar]
116. Левин М.Х., Салливан С., Нильсон Д., Ян Б., Финкбайнер В.Е., Веркман А.С. Гипертоническая солевая терапия при муковисцидозе: доказательства против предполагаемого механизма с участием аквапоринов.
 Дж. Биол. Хим. 2006; 281:25803–25812. [PubMed] [Академия Google]
Дж. Биол. Хим. 2006; 281:25803–25812. [PubMed] [Академия Google]117. Шридхарани М., Мэксон Т.Р. Промывание легких у пациента с астматическим статусом, получающего искусственную вентиляцию легких: клинический случай. Энн Аллергия. 1982; 49: 156–158. [PubMed] [Google Scholar]
118. Декрамер М., Янссенс В. Мукоактивная терапия при ХОБЛ. Eur Respir Rev. 2010; 19: 134–140. [Бесплатная статья PMC] [PubMed] [Google Scholar]
119. Rao S, Wilson DB, Brooks RC, Sproule BJ. Острые эффекты распыления N-ацетилцистеина на легочную механику и газообмен. Ам преподобный Респир Дис. 1970;102:17–22. [PubMed] [Google Scholar]
120. Minasian C, Wallis C, Metcalfe C, Bush A. Сравнение вдыхаемого маннита, ежедневного приема рчДНазы и их комбинации у детей с муковисцидозом: рандомизированное исследование. грудная клетка. 2010;65:51–56. [PubMed] [Google Scholar]
121. Seemungal TA, Wilkinson TM, Hurst JR, Perera WR, Sapsford RJ, Wedzicha JA. Длительная терапия эритромицином связана с уменьшением частоты обострений хронической обструктивной болезни легких.
 Am J Respir Crit Care Med. 2008;178:1139–1147. [PubMed] [Google Scholar]
Am J Respir Crit Care Med. 2008;178:1139–1147. [PubMed] [Google Scholar]122. Daniels JM, Snijders D, de Graaff CS, Vlaspolder F, Jansen HM, Boersma WG. Антибиотики в дополнение к системным кортикостероидам при острых обострениях хронической обструктивной болезни легких. Am J Respir Crit Care Med. 2010; 181:150–157. [PubMed] [Google Scholar]
123. Анвар Г.А., Бурк С.К., Афолаби Г., Миддлтон П., Уорд С., Резерфорд Р.М. Эффекты длительного приема низких доз азитромицина у пациентов с бронхоэктазами без муковисцидоза. Респир Мед. 2008;102:1494–1496. [PubMed] [Google Scholar]
124. Смит А.Р., Бхатт Дж. Однократное и многократное ежедневное введение аминогликозидов внутривенно при муковисцидозе. Кокрановская система базы данных, ред. 2010; 1:CD002009. [PubMed] [Google Scholar]
125. McCoy KS, Quittner AL, Oermann CM, Gibson RL, Retsch-Bogart GZ, Montgomery AB. Ингаляционный азтреонам-лизин при хронической синегнойной палочке дыхательных путей при муковисцидозе.



 Если у вас есть бактериальная инфекция или аллергия, ваш врач может назначить лекарства, чтобы облегчить воспаление и отек, а также уменьшить выработку слизи.
Если у вас есть бактериальная инфекция или аллергия, ваш врач может назначить лекарства, чтобы облегчить воспаление и отек, а также уменьшить выработку слизи. Позаботьтесь о себе домашними средствами, чтобы разжижить густые выделения, и обратитесь к врачу, если ваши симптомы не улучшатся.
Позаботьтесь о себе домашними средствами, чтобы разжижить густые выделения, и обратитесь к врачу, если ваши симптомы не улучшатся.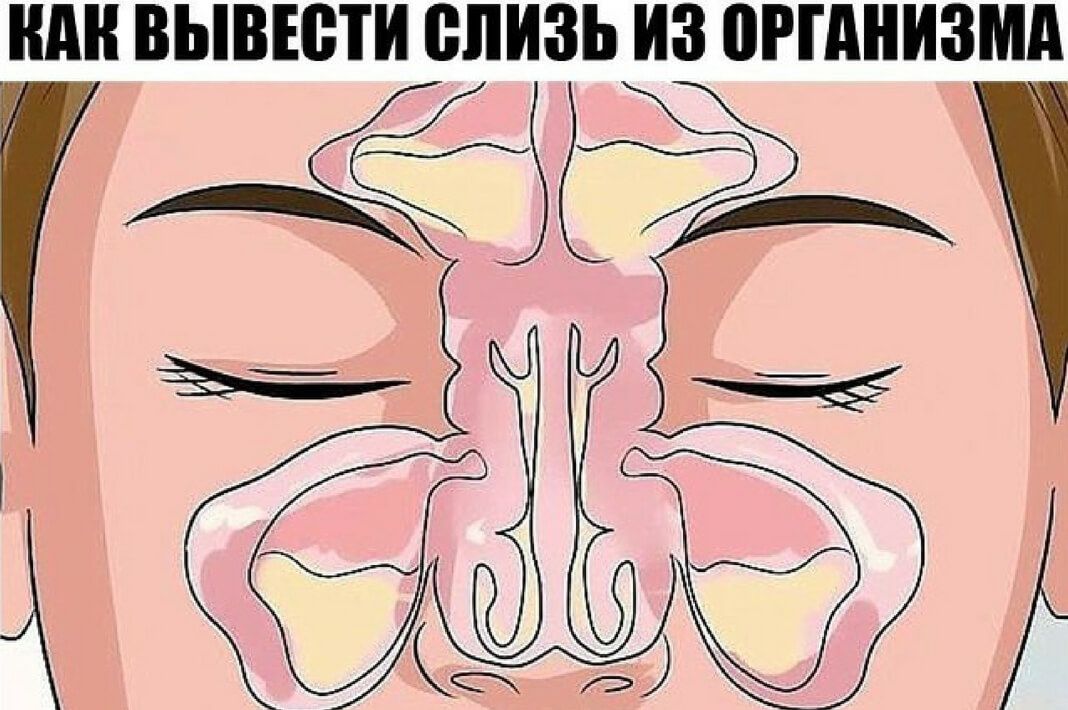
 Annu Rev Physiol. 2008; 70: 431–457. [PubMed] [Google Scholar]
Annu Rev Physiol. 2008; 70: 431–457. [PubMed] [Google Scholar] Муцин продуцируется клетками Клара в проксимальных дыхательных путях мышей, зараженных антигеном. Am J Respir Cell Mol Biol. 2004; 31: 382–394. [PubMed] [Google Scholar]
Муцин продуцируется клетками Клара в проксимальных дыхательных путях мышей, зараженных антигеном. Am J Respir Cell Mol Biol. 2004; 31: 382–394. [PubMed] [Google Scholar]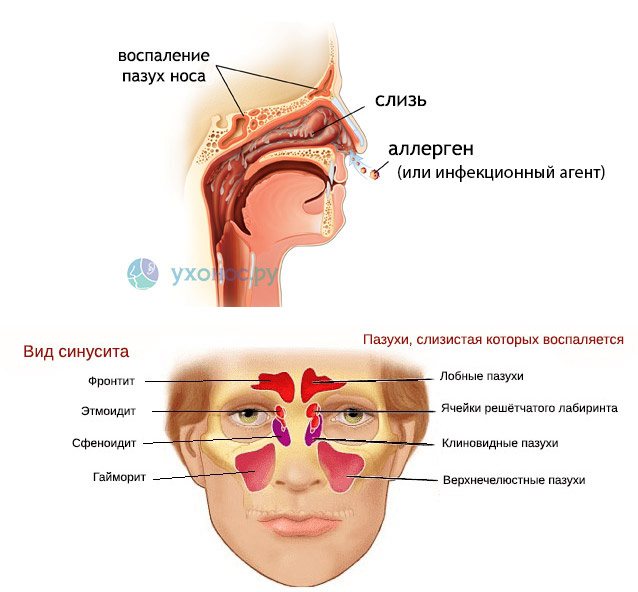 2009; 296:L92–L100. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2009; 296:L92–L100. [Бесплатная статья PMC] [PubMed] [Google Scholar]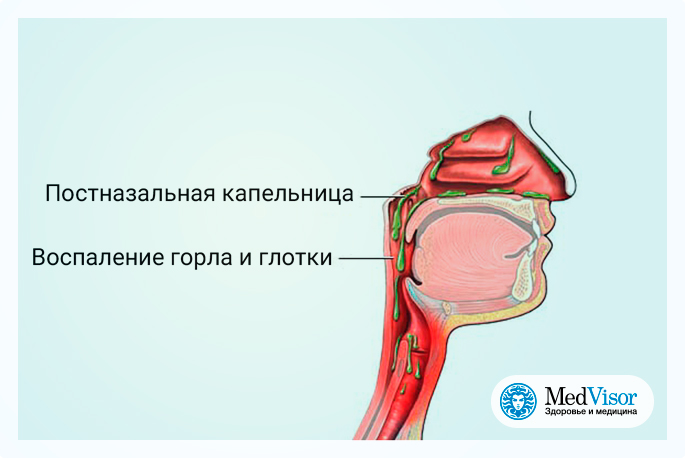 2006; 174:1018–1024. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2006; 174:1018–1024. [Бесплатная статья PMC] [PubMed] [Google Scholar] Curr Opin Struct Biol. 2008; 18: 567–576. [PubMed] [Google Scholar]
Curr Opin Struct Biol. 2008; 18: 567–576. [PubMed] [Google Scholar]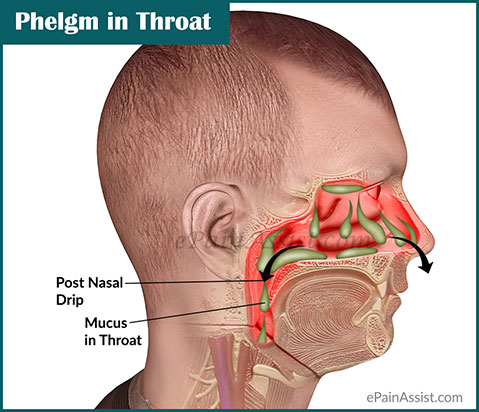 Иммунные пути перевода вирусной инфекции в хроническое заболевание дыхательных путей. Ад Иммунол. 2009; 102: 245–276. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Иммунные пути перевода вирусной инфекции в хроническое заболевание дыхательных путей. Ад Иммунол. 2009; 102: 245–276. [Бесплатная статья PMC] [PubMed] [Google Scholar] Woodruff PG, Modrek B, Choy DF, et al. Воспаление, вызываемое Т-хелперами 2 типа, определяет основные субфенотипы астмы. Am J Respir Crit Care Med. 2009; 180:388–395. [Ошибка, Am J Respir Crit Care Med 2009; 180:796.] [Бесплатная статья PMC] [PubMed] [Google Scholar]
Woodruff PG, Modrek B, Choy DF, et al. Воспаление, вызываемое Т-хелперами 2 типа, определяет основные субфенотипы астмы. Am J Respir Crit Care Med. 2009; 180:388–395. [Ошибка, Am J Respir Crit Care Med 2009; 180:796.] [Бесплатная статья PMC] [PubMed] [Google Scholar] 2006; 130:1102–1108. [PubMed] [Google Scholar]
2006; 130:1102–1108. [PubMed] [Google Scholar] [PubMed] [Академия Google]
[PubMed] [Академия Google] А. Отсутствие комплементарного рецептора анафилатоксина C3a подавляет эффекторные функции Th3 в мышиной модели легочной аллергии. Дж Иммунол. 2002; 169: 5926–5933. [PubMed] [Google Scholar]
А. Отсутствие комплементарного рецептора анафилатоксина C3a подавляет эффекторные функции Th3 в мышиной модели легочной аллергии. Дж Иммунол. 2002; 169: 5926–5933. [PubMed] [Google Scholar] Curran DR, Cohn L. Успехи в метаплазии слизистых клеток: пробка для слизи как терапевтический фокус при хроническом заболевании дыхательных путей. Am J Respir Cell Mol Biol. 2010; 42: 268–275. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Curran DR, Cohn L. Успехи в метаплазии слизистых клеток: пробка для слизи как терапевтический фокус при хроническом заболевании дыхательных путей. Am J Respir Cell Mol Biol. 2010; 42: 268–275. [Бесплатная статья PMC] [PubMed] [Google Scholar] IL-6 необходим для образования слизи в дыхательных путях, вызванной вдыхаемыми грибковыми аллергенами. Дж Иммунол. 2009 г.;183:1732–1738. [Бесплатная статья PMC] [PubMed] [Google Scholar]
IL-6 необходим для образования слизи в дыхательных путях, вызванной вдыхаемыми грибковыми аллергенами. Дж Иммунол. 2009 г.;183:1732–1738. [Бесплатная статья PMC] [PubMed] [Google Scholar] Респир Физиол Нейробиол. 2008; 163: 208–213. [Бесплатная статья PMC] [PubMed] [Google Scholar]
Респир Физиол Нейробиол. 2008; 163: 208–213. [Бесплатная статья PMC] [PubMed] [Google Scholar] Annu Rev Physiol. 2010;72:437–462. [PubMed] [Google Scholar]
Annu Rev Physiol. 2010;72:437–462. [PubMed] [Google Scholar] Int J Biochem Cell Biol. 2007;39: 1943–1954. [PubMed] [Google Scholar]
Int J Biochem Cell Biol. 2007;39: 1943–1954. [PubMed] [Google Scholar] Роу С.М., Миллер С., Соршер Э.Дж. Муковисцидоз. N Engl J Med. 2005; 352:1992–2001. [PubMed] [Академия Google]
Роу С.М., Миллер С., Соршер Э.Дж. Муковисцидоз. N Engl J Med. 2005; 352:1992–2001. [PubMed] [Академия Google] Уменьшение вязкости муковисцидозной мокроты in vitro гельсолином. Наука. 1994; 263:969–971. [PubMed] [Академия Google]
Уменьшение вязкости муковисцидозной мокроты in vitro гельсолином. Наука. 1994; 263:969–971. [PubMed] [Академия Google] Am J Respir Cell Mol Biol. 1995; 13: 748–756. [PubMed] [Академия Google]
Am J Respir Cell Mol Biol. 1995; 13: 748–756. [PubMed] [Академия Google] Глобальная инициатива по хронической обструктивной болезни легких. обновления 2009 года. (http://www.goldcopd.com.) [Google Scholar]
Глобальная инициатива по хронической обструктивной болезни легких. обновления 2009 года. (http://www.goldcopd.com.) [Google Scholar] 2006; 173:1139–1144. [PubMed] [Google Scholar]
2006; 173:1139–1144. [PubMed] [Google Scholar] 2009 г.;180:802–808. [PubMed] [Google Scholar]
2009 г.;180:802–808. [PubMed] [Google Scholar] 2009; 1:CD000996. [PubMed] [Google Scholar]
2009; 1:CD000996. [PubMed] [Google Scholar] Маркеры секреции слизи и уровни ДНК в индуцированной мокроте больных астмой и здоровых людей. Ам преподобный Респир Дис. 1993; 147:1132–1137. [PubMed] [Google Scholar]
Маркеры секреции слизи и уровни ДНК в индуцированной мокроте больных астмой и здоровых людей. Ам преподобный Респир Дис. 1993; 147:1132–1137. [PubMed] [Google Scholar] Дж. Биол. Хим. 2006; 281:25803–25812. [PubMed] [Академия Google]
Дж. Биол. Хим. 2006; 281:25803–25812. [PubMed] [Академия Google] Am J Respir Crit Care Med. 2008;178:1139–1147. [PubMed] [Google Scholar]
Am J Respir Crit Care Med. 2008;178:1139–1147. [PubMed] [Google Scholar]