Содержание
Как определить стеноз гортани | Справочник медицинской лаборатории Оптимум (Сочи, Адлер)
Получить результаты анализов
- Главная
- Как распознать болезнь
- Заболевания органов дыхания
- Стеноз гортани
Подробнее о враче
Стеноз гортани – это патологическое состояние, характеризующее сужением гортани, которое препятствует поступлению кислорода. Носит острый и хронический характер, острый стеноз возникает за несколько недель и протекает стремительно, хронический формируется больше 4 недель. Болезнь диагностируется как у взрослых, так и детей.
Формы стеноза
Патология имеет несколько основных форм, которые выделяют с учетом причин, вызвавших заболевание:
- паралитический. Возникает в связи с нарушением проведения нервного импульса;
- рубцовый.
 Причиной такой формы являются инфекционные болезни, травмы гортани после операций и ранений, длительная процедура искусственной вентиляции;
Причиной такой формы являются инфекционные болезни, травмы гортани после операций и ранений, длительная процедура искусственной вентиляции; - опухолевый. Патологическое состояние появляется на фоне доброкачественных и злокачественных образований.
Кроме этого, в зависимости от локализации болезни, различаются такие стенозы как протяженный, круговой, подголосового пространства и пр.
Причины развития
Влияют на образования стеноза следующие основные факторы:
- черепно-мозговые травмы;
- операционное вмешательство на гортани и ее ожоги;
- опухолевые образования щитовидной железы;
- аллергия;
- тяжелые инфекционные патологи органов дыхания;
- применение лучевой терапии;
- наличие рубцов гортани.
Развитию стеноза в детском возрасте способствует особенность строения гортани, в связи с этим симптоматика болезни нередко проявляется во время простуды либо при аллергической реакции.
Симптомы и первые признаки
При первых проявлениях недуга у больных возникают трудности с дыханием, отдышка, замедляется ритм сердца. С прогрессированием затрудняется выдох, дыхание становится свистящим, повышается АД, бледнеет кожа, постоянно присутствует отдышка. Наиболее опасная – это тяжелая форма, когда происходит остановка дыхания, начинаются судороги, прекращается работа сердца. В данном случае больному необходима срочная медицинская помощь.
Методы диагностики
Диагностические мероприятия включают:
- общий осмотр и выслушивания жалоб пациента;
- обследование функционирования внешнего дыхания;
- проведение ларингоскопии;
- использование эндоскопии, когда с помощью эндоскопа изучается просвет гортани.
Если специалист затрудняется при постановке диагноза, рекомендуется пройти ультразвуковое исследование щитовидки, КРТ и МРТ, обследование зева на наличие бактерий и вирусов.
Лечение
Первая помощь при стенозе гортани заключается в вызове скорой помощи, а до приезда специалистов рекомендуют больному придать полусидящее положение, освободить грудную клетку, дать доступ свежего воздуха. В зависимости от причины, вызывающей заболевание, назначаются антигистаминные и антибактериальные средства, осуществляется противовирусная терапия, извлекаются инородные тела с гортани и пр. В определенных случаях прибегают к оперативному вмешательству, где во время операции удаляются рубцы, опухоли, проводиться имплантация стентов, предупреждающие сужение.
В зависимости от причины, вызывающей заболевание, назначаются антигистаминные и антибактериальные средства, осуществляется противовирусная терапия, извлекаются инородные тела с гортани и пр. В определенных случаях прибегают к оперативному вмешательству, где во время операции удаляются рубцы, опухоли, проводиться имплантация стентов, предупреждающие сужение.
Современные методы профилактики и терапии осложнений при реконструктивной хирургии у пациентов со стенозом гортани и трахеи
Лечение пациентов со стенозом гортани и трахеи в настоящее время является актуальной проблемой оториноларингологии. Несмотря на большое количество методов лечения больных с данной патологией, алгоритмы терапии и по сей день требуют детального анализа [1, 2].
Как известно, хронический стеноз гортани и трахеи — жизнеугрожающее состояние, представляющее собой сужение просвета дыхательных путей, ведущее к снижению вентиляции легких и системной гипоксии. Среди причин, вызывающих данную патологию, выделяют травматические, аутоиммунные, идиопатические, ятрогенные, новообразования и др. [3].
[3].
Рассматривая данные патологические состояния, стоит выделить хронические рубцовые стенозы гортани и трахеи, в патогенезе которых основная роль принадлежит сужению дыхательных путей в результате образования рубцовой ткани, что отрицательно влияет на голосовые и коммуникативные способности, нарушает респираторную поддержку и может привести к критическим, опасным для жизни осложнениям. В зависимости от степени выраженности стриктуры симптомы могут варьировать от легкой одышки при физической нагрузке, дисфонии и стридора, до серьезных респираторных расстройств из-за обструкции дыхательных путей [4].
В настоящее время существует множество методов хирургического лечения больных стенозом гортани и трахеи, основной целью которых является восстановление просвета дыхательных путей. Несмотря на разнообразие данных методов, в послеоперационном периоде у больных стенозом гортани и трахеи встречается ряд осложнений, из которых, по данным некоторых исследователей, более 60% обусловлено развитием гнойно-воспалительных процессов. Этому способствует ряд факторов, таких как этиология стеноза, наличие хронического воспалительного процесса или предшествующая контаминация области операции, объем проведенного оперативного лечения, повторные хирургические вмешательства, а также коморбидные состояния и др. [2, 3].
Этому способствует ряд факторов, таких как этиология стеноза, наличие хронического воспалительного процесса или предшествующая контаминация области операции, объем проведенного оперативного лечения, повторные хирургические вмешательства, а также коморбидные состояния и др. [2, 3].
Большинство случаев хронических рубцовых стенозов гортани и трахеи связано с ятрогенными причинами, такими как интубационная травма или трахеотомия, которые провоцируют повреждение эпителия. Рубцовая ткань может также формироваться в результате аутоиммунного заболевания или очаговой травмы. Стенозы, причину которых установить не удается, относят к идиопатическим [4].
Несмотря на разницу в этиологии описанных типов рубцового стеноза, общей их характеристикой является воспаление слизистой оболочки. В основе патогенеза хронических рубцовых стенозов гортани и трахеи лежит аберрантный механизм заживления. Суть данного процесса заключается в травматизации эпителия, что приводит к развитию субэпителиального воспаления. В свою очередь в собственной пластинке слизистой оболочки воспаление вызывает пролиферацию фибробластов, которые продуцируют белки внеклеточного матрикса, способствующие последующему отложению грануляционной ткани и образованию рубцов. В случае ларинготрахеального стеноза это субэпителиальное воспаление, как полагают, опосредовано Т-лимфоцитами с преобладанием профибротических цитокинов, способствующих чрезмерному отложению рубцовой ткани. Исследования, в ходе которых проводили изучение гистологической структуры тканей, специфичных для стеноза гортани и трахеи, выявили усиление васкуляризации в грануляционной ткани, фиброз с утолщенным связыванием коллагена, атрофию слизистых протоков и желез, а также воспалительное изъязвление. Аналогичные изменения возникают в слизистой оболочке гортани и трахеи у пациентов, перенесших реконструктивные вмешательства, в послеоперационном периоде [4].
В свою очередь в собственной пластинке слизистой оболочки воспаление вызывает пролиферацию фибробластов, которые продуцируют белки внеклеточного матрикса, способствующие последующему отложению грануляционной ткани и образованию рубцов. В случае ларинготрахеального стеноза это субэпителиальное воспаление, как полагают, опосредовано Т-лимфоцитами с преобладанием профибротических цитокинов, способствующих чрезмерному отложению рубцовой ткани. Исследования, в ходе которых проводили изучение гистологической структуры тканей, специфичных для стеноза гортани и трахеи, выявили усиление васкуляризации в грануляционной ткани, фиброз с утолщенным связыванием коллагена, атрофию слизистых протоков и желез, а также воспалительное изъязвление. Аналогичные изменения возникают в слизистой оболочке гортани и трахеи у пациентов, перенесших реконструктивные вмешательства, в послеоперационном периоде [4].
В настоящее время также не вызывает сомнений роль микроорганизмов в генезе воспалительного процесса, связанного с рубцовыми стенозами гортани и трахеи. Этот факт подтвержден научными работами, демонстрирующими связи стеноза с контаминацией слизистой оболочки бактериальной микрофлорой, включая нозокомиальную инфекцию. Прогресс в молекулярных технологиях за последние годы позволил исследовать факторы воспаления, выявив аберрантную активацию в пути воспаления интерлейкина-17A и интерлейкина-23 в слизистой оболочке при идиопатическом рубцовом подскладковом стенозе. Основным продуцентом интерлейкина-17A является подтип T-клеток, распознающих микробные антигены, что в очередной раз подтверждает роль микроорганизмов в развитии стенотических состояний. Последние достижения в области секвенирования генома микроорганизмов позволяют проводить профилирование структуры всего микробного сообщества, что позволило более детально изучить роль микробиома в физиологии и патологии верхних и нижних дыхательных путей. Одно из недавно проведенных исследований, в котором изучалась микрофлора слизистой оболочки у пациентов со стенозом гортани и трахеи, показало, что бактерии рода Acinetobacter, идентифицированные по результатам ПЦР, имеют связь с ятрогенными подскладковыми стенозами, а Mycobacterium — с идиопатическим подскладковым рубцовым стенозом.
Этот факт подтвержден научными работами, демонстрирующими связи стеноза с контаминацией слизистой оболочки бактериальной микрофлорой, включая нозокомиальную инфекцию. Прогресс в молекулярных технологиях за последние годы позволил исследовать факторы воспаления, выявив аберрантную активацию в пути воспаления интерлейкина-17A и интерлейкина-23 в слизистой оболочке при идиопатическом рубцовом подскладковом стенозе. Основным продуцентом интерлейкина-17A является подтип T-клеток, распознающих микробные антигены, что в очередной раз подтверждает роль микроорганизмов в развитии стенотических состояний. Последние достижения в области секвенирования генома микроорганизмов позволяют проводить профилирование структуры всего микробного сообщества, что позволило более детально изучить роль микробиома в физиологии и патологии верхних и нижних дыхательных путей. Одно из недавно проведенных исследований, в котором изучалась микрофлора слизистой оболочки у пациентов со стенозом гортани и трахеи, показало, что бактерии рода Acinetobacter, идентифицированные по результатам ПЦР, имеют связь с ятрогенными подскладковыми стенозами, а Mycobacterium — с идиопатическим подскладковым рубцовым стенозом. По данным A. Hillel и соавт. [4], при хроническом рубцовом стенозе гортани и трахеи выделялись бактерии семейств Prevotellaceae, Streptococcaceae, Veillonellaceae, Neisseriaceae и Pasteurellaceae с преобладанием родов Bacteroides, Clostridium, Bacillus, Gammaproteobacteria и Betaproteobacteria. При бактериологическом исследовании раневого отделяемого после выполнения реконструктивных операций на гортани и трахее, по данным ряда авторов, высеивались различные виды стафилококков, на 14-е сутки после операции в 30% случаев отмечалось появление новых видов микроорганизмов — P. aeruginosa, Candida и др. [5]. По данным других авторов, при бактериологических исследованиях у пациентов с послеоперационным инфицированием отмечается рост S. aureus, часто полирезистентого, и/или P. aeruginosa, а также ряда других патогенов, включая различных представителей рода Streptococcus и E. coli. Учитывая непосредственное участие микроорганизмов в патогенезе рубцовых стенозов и осложнений при реконструктивных хирургических вмешательствах, становится очевидной необходимость рационального подхода как к антибиотикопрофилактике, так и к антибактериальной терапии у данной категории больных, при этом ввиду определенных факторов устойчивости микроорганизмов данный вопрос остается открытым [6].
По данным A. Hillel и соавт. [4], при хроническом рубцовом стенозе гортани и трахеи выделялись бактерии семейств Prevotellaceae, Streptococcaceae, Veillonellaceae, Neisseriaceae и Pasteurellaceae с преобладанием родов Bacteroides, Clostridium, Bacillus, Gammaproteobacteria и Betaproteobacteria. При бактериологическом исследовании раневого отделяемого после выполнения реконструктивных операций на гортани и трахее, по данным ряда авторов, высеивались различные виды стафилококков, на 14-е сутки после операции в 30% случаев отмечалось появление новых видов микроорганизмов — P. aeruginosa, Candida и др. [5]. По данным других авторов, при бактериологических исследованиях у пациентов с послеоперационным инфицированием отмечается рост S. aureus, часто полирезистентого, и/или P. aeruginosa, а также ряда других патогенов, включая различных представителей рода Streptococcus и E. coli. Учитывая непосредственное участие микроорганизмов в патогенезе рубцовых стенозов и осложнений при реконструктивных хирургических вмешательствах, становится очевидной необходимость рационального подхода как к антибиотикопрофилактике, так и к антибактериальной терапии у данной категории больных, при этом ввиду определенных факторов устойчивости микроорганизмов данный вопрос остается открытым [6].
В настоящее время считают, что в естественных и искусственно созданных окружающих средах большинство микроорганизмов существует в виде биопленок, образование которых является одним из главных механизмов их выживания в окружающей среде. Биопленки присоединяются к живой или неживой поверхности с помощью синтезируемого микроорганизмами полисахаридного матрикса, при этом количество микробных клеток составляет лишь от 5 до 35% массы биопленок. Поверхностная оболочка биопленки состоит из билипидного слоя, повышенная прочность которого обеспечивается бо́льшим количеством кардиолипина, чем у мембран бактериальных клеток. Матрикс представляет собой смесь нескольких компонентов: липополисахаридов, гликопротеидов, протеогликанов, нуклеиновых кислот и других веществ, аналогичных по составу мембранным образованиям бактерий. Микроколонии бактерий, погруженные в межклеточный матрикс, имеют свои микросреды, отличающиеся концентрацией кислорода, уровнями кислотности, усвоением питательных веществ. Матрикс пронизан каналами, по которым циркулируют ферменты, питательные вещества, кислород и продукты жизнедеятельности микроорганизмов. Биопленки — подвижные, непрерывно изменяющиеся гетерогенные сообщества, которые могут как состоять из одного вида бактерий, так и содержать в себе многочисленные разнообразные виды микроорганизмов. По данным отечественных и зарубежных исследователей, более 60% случаев внутрибольничных инфекций вызвано бактериями, находящимися в биопленках. Устойчивость к антибактерильным и антисептическим препаратам у формирующих биопленки микроорганизмов реализуется несколькими механизмами. Во-первых, проникновение антибактериальных препаратов в основное вещество биопленки замедляется за счет связывания с полисахаридными компонентами матрикса. Во-вторых, в составе биопленок бактерии находятся в разной метаболической активности: на периферии биопленок располагаются метаболически более активные клетки, а внутри — неактивные. Так как антибиотики воздействуют только на активно растущие клетки, микроорганизмы, находящиеся внутри биопленок, оказываются защищенными.
Матрикс пронизан каналами, по которым циркулируют ферменты, питательные вещества, кислород и продукты жизнедеятельности микроорганизмов. Биопленки — подвижные, непрерывно изменяющиеся гетерогенные сообщества, которые могут как состоять из одного вида бактерий, так и содержать в себе многочисленные разнообразные виды микроорганизмов. По данным отечественных и зарубежных исследователей, более 60% случаев внутрибольничных инфекций вызвано бактериями, находящимися в биопленках. Устойчивость к антибактерильным и антисептическим препаратам у формирующих биопленки микроорганизмов реализуется несколькими механизмами. Во-первых, проникновение антибактериальных препаратов в основное вещество биопленки замедляется за счет связывания с полисахаридными компонентами матрикса. Во-вторых, в составе биопленок бактерии находятся в разной метаболической активности: на периферии биопленок располагаются метаболически более активные клетки, а внутри — неактивные. Так как антибиотики воздействуют только на активно растущие клетки, микроорганизмы, находящиеся внутри биопленок, оказываются защищенными.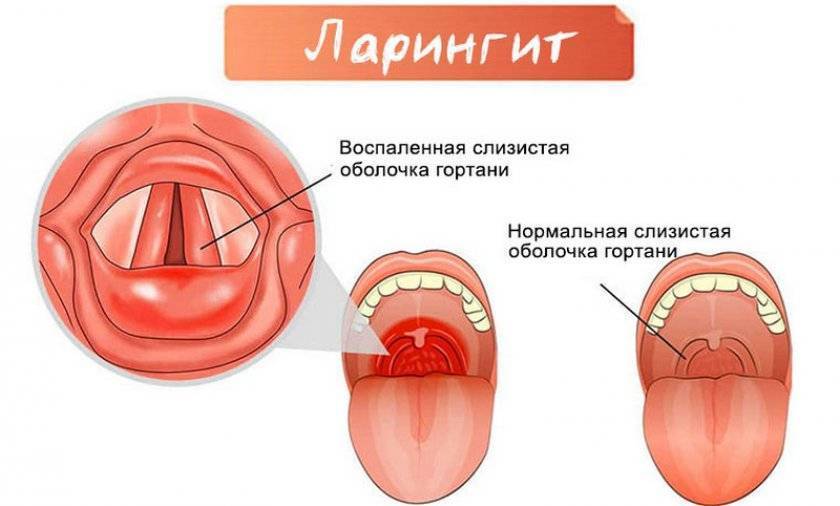 В-третьих, в составе биопленок свободная поверхность бактерий уменьшается за счет контактов друг с другом. Таким образом, после воздействия антибактериальных препаратов остаются жизнеспособные бактерии, приобретающие устойчивость к антибиотикам. Количество этих бактерий, называемых персисторами, в составе биопленок варьирует от 1 до 10%. Особый интерес представляет антибиотикорезистентность полимикробных биопленок, в которых устойчивые бактерии вырабатывают защитные энзимы и связывающие антибиотики протеины, защищающие антибиотикочувствительные бактерии. Кроме того, различные виды образующих биопленку бактерий несут различное сочетание генов резистентности и способны передавать эти гены друг другу в условиях тесного контакта.
В-третьих, в составе биопленок свободная поверхность бактерий уменьшается за счет контактов друг с другом. Таким образом, после воздействия антибактериальных препаратов остаются жизнеспособные бактерии, приобретающие устойчивость к антибиотикам. Количество этих бактерий, называемых персисторами, в составе биопленок варьирует от 1 до 10%. Особый интерес представляет антибиотикорезистентность полимикробных биопленок, в которых устойчивые бактерии вырабатывают защитные энзимы и связывающие антибиотики протеины, защищающие антибиотикочувствительные бактерии. Кроме того, различные виды образующих биопленку бактерий несут различное сочетание генов резистентности и способны передавать эти гены друг другу в условиях тесного контакта.
Стоит отметить, что присутствие стафилококковой биопленки в опыте на мышах значительно снижает скорость эпителизации ран. Так, по данным литературы, у 75% пациентов, у которых выделяли S. аureus, наблюдалось повышенное образование грануляционной ткани вокруг трахеостомы и в просвете трахеи. При этом рост грануляционной ткани у пациентов, перенесших хирургическое вмешательство на гортани и трахее, в значительной степени зависит от наличия воспалительной реакции в области операции, а контаминация этой области патогенной флорой усугубляет данную реакцию. Таким образом, учитывая изложенные механизмы резистентности микроорганизмов, одним из важнейших звеньев периоперационного ведения больных со стенозом гортани и трахеи становятся антимикробная профилактика и терапия гнойно-воспалительных осложнений [7—9].
При этом рост грануляционной ткани у пациентов, перенесших хирургическое вмешательство на гортани и трахее, в значительной степени зависит от наличия воспалительной реакции в области операции, а контаминация этой области патогенной флорой усугубляет данную реакцию. Таким образом, учитывая изложенные механизмы резистентности микроорганизмов, одним из важнейших звеньев периоперационного ведения больных со стенозом гортани и трахеи становятся антимикробная профилактика и терапия гнойно-воспалительных осложнений [7—9].
Лечение больных с хроническими стенозами гортани и трахеи, по мнению многих авторов, должно быть сосредоточено на купировании воспалительного процесса в послеоперационном периоде, а также на приостановлении прогрессирования процесса формирования грубоволокнистой соединительной ткани, влекущего за собой образование рубцового стеноза. Большинство методов консервативной терапии рубцовых стенозов гортани и трахеи направлено на купирование бактериального воспаления в дыхательных путях, а также на ускорение процессов раневого заживления после реконструктивных операций.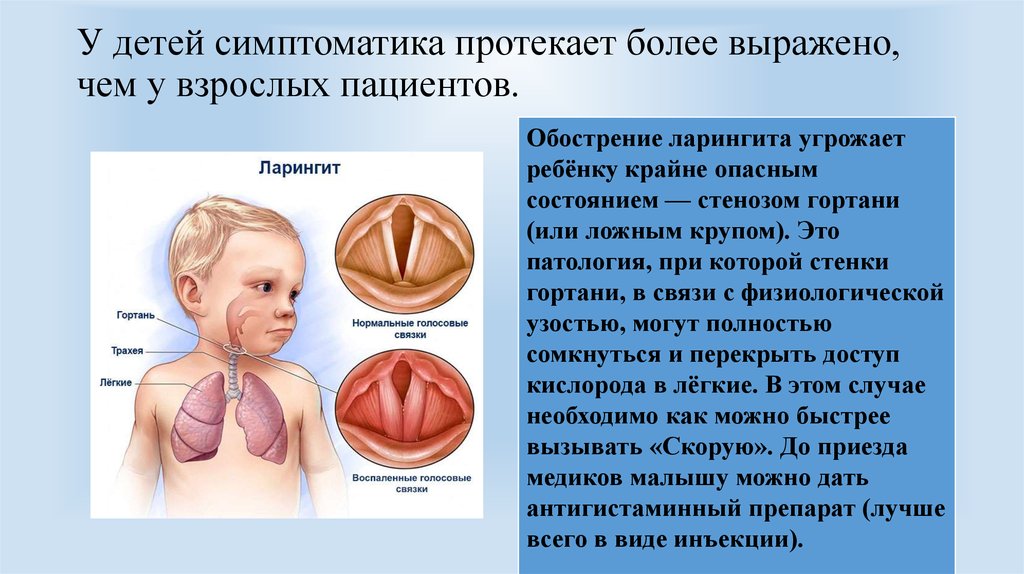 Для послеоперационного лечения больных стенозом гортани и трахеи многие исследователи применяли физиотерапевтическое лечение. Авторы отмечали улучшение микроциркуляции при применении низкочастотной магнитотерапии. Стоит отметить лечебный эффект лазерного излучения, обусловленный антибактериальным, противоотечным, противовоспалительным, аналгезирующим, иммунокорригирующим действием, стимуляцией окислительно-восстановительных процессов, усилением микроциркуляции, повышением энергетического и пластического обмена [10, 11]. По данным авторов, применение лазерной терапии с использованием низкоинтенсивного инфракрасного излучения импульсного воздействия позволяет снизить количество послеоперационных гнойно-воспалительных осложнений в 2,5 раза. Некоторые исследователи использовали комплексный подход к лечению с применением антибактериальных препаратов, противоотечной и десенсибилизирующей терапии, иммуностимуляторов, гипербарической оксигенации и лазертерапии [12]. В связи с открытием свойств оксида азота в последние годы появились сообщения об использовании экзогенной NО-терапии в послеоперационном ведении больных с хроническими рубцовыми стенозами гортани и трахеи.
Для послеоперационного лечения больных стенозом гортани и трахеи многие исследователи применяли физиотерапевтическое лечение. Авторы отмечали улучшение микроциркуляции при применении низкочастотной магнитотерапии. Стоит отметить лечебный эффект лазерного излучения, обусловленный антибактериальным, противоотечным, противовоспалительным, аналгезирующим, иммунокорригирующим действием, стимуляцией окислительно-восстановительных процессов, усилением микроциркуляции, повышением энергетического и пластического обмена [10, 11]. По данным авторов, применение лазерной терапии с использованием низкоинтенсивного инфракрасного излучения импульсного воздействия позволяет снизить количество послеоперационных гнойно-воспалительных осложнений в 2,5 раза. Некоторые исследователи использовали комплексный подход к лечению с применением антибактериальных препаратов, противоотечной и десенсибилизирующей терапии, иммуностимуляторов, гипербарической оксигенации и лазертерапии [12]. В связи с открытием свойств оксида азота в последние годы появились сообщения об использовании экзогенной NО-терапии в послеоперационном ведении больных с хроническими рубцовыми стенозами гортани и трахеи. С данной целью использовали воздушно-плазменный аппарат Плазон, способный генерировать экзогенный оксид азота, применение которого позволяет на несколько дней сократить срок заживления послеоперационных ран. Среди эффектов NO-терапии отмечались бактерицидный эффект, нормализация микроциркуляции послеоперационной области, снижение выраженности воспалительных явлений, усиление фагоцитоза и макрофагеальной реакции, ускорение пролиферации фибробластов [13]. Обращает на себя внимание возросший интерес к использованию современных мукоактивных препаратов для терапии больных с хроническими рубцовыми стенозами гортани и трахеи. Данные препараты обладают рядом свойств, таких как нарушение адгезии микробных клеток к твердой поверхности, бактерицидная, бактериостатическая и муколитическая активность, что позволяет рассматривать их в качестве эффективного средства терапии у данной категории больных. Так, Е.В. Егорова [14] проводила интратрахеальное подслизистое введение флуимуцил-антибиотика в дозировке 500 мг и полиоксидония в дозировке 0,006 мг у 42 пациентов с данной патологией.
С данной целью использовали воздушно-плазменный аппарат Плазон, способный генерировать экзогенный оксид азота, применение которого позволяет на несколько дней сократить срок заживления послеоперационных ран. Среди эффектов NO-терапии отмечались бактерицидный эффект, нормализация микроциркуляции послеоперационной области, снижение выраженности воспалительных явлений, усиление фагоцитоза и макрофагеальной реакции, ускорение пролиферации фибробластов [13]. Обращает на себя внимание возросший интерес к использованию современных мукоактивных препаратов для терапии больных с хроническими рубцовыми стенозами гортани и трахеи. Данные препараты обладают рядом свойств, таких как нарушение адгезии микробных клеток к твердой поверхности, бактерицидная, бактериостатическая и муколитическая активность, что позволяет рассматривать их в качестве эффективного средства терапии у данной категории больных. Так, Е.В. Егорова [14] проводила интратрахеальное подслизистое введение флуимуцил-антибиотика в дозировке 500 мг и полиоксидония в дозировке 0,006 мг у 42 пациентов с данной патологией. Через 14 дней после данной манипуляции обнаруживали восстановление мерцательного эпителия слизистой оболочки гортани и трахеи. В.Н. Фоломеев [15] предлагал при помощи ультразвука вводить пациентам в предоперационном периоде протэгентин — комбинированный препарат, имеющий в составе гентамицин и эритромицин, а также протеолитический фермент (протеазу С). По данным автора, концентрация этого препарата в тканях операционной области снижает количество послеоперационных осложнений на 16%, значительно уменьшая выраженность послеоперационного воспаления и рост грануляционной ткани. По мнению ряда авторов, соединительная ткань обладает иммунной реактивностью, что обусловливает аутоиммунное течение воспалительного процесса при травме гортани и трахеи. Для уменьшения данных явлений применяется поэтапная гормонотерапия. С данной целью под контролем непрямой ларингоскопии больным проводили инъекции триамцинолона ацетонида и метилацетата преднизолона в сочетании с гиалуронидазой в область рубцов через кожу, при этом отмечалось значительное замедление формирования рубцовой ткани.
Через 14 дней после данной манипуляции обнаруживали восстановление мерцательного эпителия слизистой оболочки гортани и трахеи. В.Н. Фоломеев [15] предлагал при помощи ультразвука вводить пациентам в предоперационном периоде протэгентин — комбинированный препарат, имеющий в составе гентамицин и эритромицин, а также протеолитический фермент (протеазу С). По данным автора, концентрация этого препарата в тканях операционной области снижает количество послеоперационных осложнений на 16%, значительно уменьшая выраженность послеоперационного воспаления и рост грануляционной ткани. По мнению ряда авторов, соединительная ткань обладает иммунной реактивностью, что обусловливает аутоиммунное течение воспалительного процесса при травме гортани и трахеи. Для уменьшения данных явлений применяется поэтапная гормонотерапия. С данной целью под контролем непрямой ларингоскопии больным проводили инъекции триамцинолона ацетонида и метилацетата преднизолона в сочетании с гиалуронидазой в область рубцов через кожу, при этом отмечалось значительное замедление формирования рубцовой ткани. Также применяли внутривенное введение метилпреднизолона в дозировке 1 мг/кг у больных с паралитическими стенозами в периоперационном периоде. В дальнейшем терапия кортикостероидами была продолжена до 16 дней с постепенным снижением дозировки лекарственных препаратов. Для уменьшения отека и предупреждения рецидива стеноза также применяли курсовое лечение глюкокортикостероидами. Применение данных препаратов обусловлено их противовоспалительным, иммуносупрессивным действием [16]. При лечении рубцовых процессов различных областей многими авторами используется препарат дипроспан, действие которого начинается спустя 2—4 ч после введения, а за счет медленно действующей фракции в его составе (бетаметазона дипропионат) продолжается до 3—6 мес. Также имеются данные о внутрикожном применении дипроспана в дерматологии при лечении келлоидных рубцов. В комплексной терапии у больных стенозом гортани и трахеи с избыточным ростом грануляционной ткани в послеоперационном периоде осуществлялись инъекции дипроспана в область грануляций в дозировке 2,5 мг/мл.
Также применяли внутривенное введение метилпреднизолона в дозировке 1 мг/кг у больных с паралитическими стенозами в периоперационном периоде. В дальнейшем терапия кортикостероидами была продолжена до 16 дней с постепенным снижением дозировки лекарственных препаратов. Для уменьшения отека и предупреждения рецидива стеноза также применяли курсовое лечение глюкокортикостероидами. Применение данных препаратов обусловлено их противовоспалительным, иммуносупрессивным действием [16]. При лечении рубцовых процессов различных областей многими авторами используется препарат дипроспан, действие которого начинается спустя 2—4 ч после введения, а за счет медленно действующей фракции в его составе (бетаметазона дипропионат) продолжается до 3—6 мес. Также имеются данные о внутрикожном применении дипроспана в дерматологии при лечении келлоидных рубцов. В комплексной терапии у больных стенозом гортани и трахеи с избыточным ростом грануляционной ткани в послеоперационном периоде осуществлялись инъекции дипроспана в область грануляций в дозировке 2,5 мг/мл. При дальнейшем эндоскопическом обследовании у данных пациентов отмечался регресс процесса образования грануляционной ткани, что в свою очередь снизило риск рестенозирования трахеи. Перспективным считают использование протеаз с выраженной некролитической активностью, способных гидролизировать фибрин и активировать плазминоген. В.Э. Кокорина [17] в своей работе использует препарат коллагеназа КК (полиферментный препарат, полученный из гепатопанкреаса камчатского краба) в сочетании с дипроспаном, в виде инъекций этих препаратов в зону роста грануляционной ткани. Автор отмечает положительное действие данной терапии на мукоцилиарный клиренс слизистой оболочки трахеи и ее большую эффективность по сравнению с применением трипсина и дексаметазона. Среди методик лечения больных стенозами гортани и трахеи находят свое место применение биостимуляторов местного действия (хонсурид), а также электрофорез и фонофорез с антибактериальными мазями и препаратами для улучшения регенерации тканей, такими как солкосерил и актовегин, что способствует ускорению репарации [15].
При дальнейшем эндоскопическом обследовании у данных пациентов отмечался регресс процесса образования грануляционной ткани, что в свою очередь снизило риск рестенозирования трахеи. Перспективным считают использование протеаз с выраженной некролитической активностью, способных гидролизировать фибрин и активировать плазминоген. В.Э. Кокорина [17] в своей работе использует препарат коллагеназа КК (полиферментный препарат, полученный из гепатопанкреаса камчатского краба) в сочетании с дипроспаном, в виде инъекций этих препаратов в зону роста грануляционной ткани. Автор отмечает положительное действие данной терапии на мукоцилиарный клиренс слизистой оболочки трахеи и ее большую эффективность по сравнению с применением трипсина и дексаметазона. Среди методик лечения больных стенозами гортани и трахеи находят свое место применение биостимуляторов местного действия (хонсурид), а также электрофорез и фонофорез с антибактериальными мазями и препаратами для улучшения регенерации тканей, такими как солкосерил и актовегин, что способствует ускорению репарации [15]. Также в последние десятилетия активно используются различные виды энзимотерапии с использованием протеаз. Протеазы не только сами напрямую влияют на раневые субстраты, но оказывают и опосредованное воздействие через активацию протеаз раневого содержимого. Группы протеаз, таких как трипсин, химотрипсин, терролитин и др., в настоящее время широко применяют для лечения гнойно-некротических ран. C целью профилактики рецидива рубцового стеноза в послеоперационном периоде использовали эластолитин и колитин — ферменты эластазного и коллагеназного действия, которые вводили при помощи электрофореза. Положительно зарекомендовал себя также препарат Ируксол, имеющий в составе коллагеназу Clostridium histolyticum [18]. Препарат Флогензим, основу которого составляют протеазы животного и растительного происхождения, показал высокую эффективность в купировании воспалительных процессов, уменьшая инфильтрацию интерстиция плазменными белками [19].
Также в последние десятилетия активно используются различные виды энзимотерапии с использованием протеаз. Протеазы не только сами напрямую влияют на раневые субстраты, но оказывают и опосредованное воздействие через активацию протеаз раневого содержимого. Группы протеаз, таких как трипсин, химотрипсин, терролитин и др., в настоящее время широко применяют для лечения гнойно-некротических ран. C целью профилактики рецидива рубцового стеноза в послеоперационном периоде использовали эластолитин и колитин — ферменты эластазного и коллагеназного действия, которые вводили при помощи электрофореза. Положительно зарекомендовал себя также препарат Ируксол, имеющий в составе коллагеназу Clostridium histolyticum [18]. Препарат Флогензим, основу которого составляют протеазы животного и растительного происхождения, показал высокую эффективность в купировании воспалительных процессов, уменьшая инфильтрацию интерстиция плазменными белками [19].
С целью профилактики чрезмерного образования рубцов в послеоперационном периоде в хирургической практике в последнее время используют препараты цитостатики, обладающие местно-прижигающим, противовоспалительным действием. Применение цитостатиков в области оперативного вмешательства за счет выраженного антипролиферативного, противовоспалительного и протекторного действия позволило добиться регресса клинических симптомов гипертрофических рубцовых деформаций у подавляющего большинства больных, независимо от длительности процесса, и повысить стабильность результатов в отдаленные сроки — до 2 лет и более. По данным Е.А. Кирасировой [1] и Р.А. Резакова [2], применение митомицина-С способствовало быстрому и эффективному заживлению слизистой оболочки в области оперативного вмешательства. При этом митомицин-С в проведенных исследованиях не оказывал негативного влияния на эпителизацию области оперативного вмешательства.
Применение цитостатиков в области оперативного вмешательства за счет выраженного антипролиферативного, противовоспалительного и протекторного действия позволило добиться регресса клинических симптомов гипертрофических рубцовых деформаций у подавляющего большинства больных, независимо от длительности процесса, и повысить стабильность результатов в отдаленные сроки — до 2 лет и более. По данным Е.А. Кирасировой [1] и Р.А. Резакова [2], применение митомицина-С способствовало быстрому и эффективному заживлению слизистой оболочки в области оперативного вмешательства. При этом митомицин-С в проведенных исследованиях не оказывал негативного влияния на эпителизацию области оперативного вмешательства.
Среди способов введения лекарственных препаратов для купирования хронических воспалительных явлений в гортани и трахее следует отдельно выделить ингаляционный. Основным преимуществом данного подхода является возможность достижения быстрого и эффективного лечебного действия лекарственного препарата с применением относительно небольшой его дозы, при этом отрицательные системные эффекты проявляются в значительно меньшей степени. Во время ингаляции происходит быстрое и интенсивное всасывание лекарственных препаратов с увеличением их активной поверхности и депонированием их в подслизистом слое. Таким образом, непосредственно в очаге воспаления создается высокая концентрация лекарственного средства. Преимуществом аэрозольтерапии также является тот факт, что частицы лекарственного вещества проникают в организм в неизмененном виде, так как минуют печень [20]. Для ингаляционной терапии в настоящее время применяются специальные приборы, небулайзеры (от лат. nebula — туман, облачко), преобразующие жидкий лекарственный препарат в аэрозоль, состоящий из микрочастиц лекарственного средства. Достижение лекарственным препаратом ингаляционной формы в небулайзерах осуществляется различными способами, что определяет возможность их применения в различных клинических ситуациях. Различают 3 основных типа небулайзеров: компрессорные, ультразвуковые и мэш-небулайзеры. В компрессорных небулайзерах образование аэрозоля достигается за счет подачи мощной струи воздуха, в ультразвуковых — за счет колебания пьезоэлектрического кристалла на ультразвуковых частотах.
Во время ингаляции происходит быстрое и интенсивное всасывание лекарственных препаратов с увеличением их активной поверхности и депонированием их в подслизистом слое. Таким образом, непосредственно в очаге воспаления создается высокая концентрация лекарственного средства. Преимуществом аэрозольтерапии также является тот факт, что частицы лекарственного вещества проникают в организм в неизмененном виде, так как минуют печень [20]. Для ингаляционной терапии в настоящее время применяются специальные приборы, небулайзеры (от лат. nebula — туман, облачко), преобразующие жидкий лекарственный препарат в аэрозоль, состоящий из микрочастиц лекарственного средства. Достижение лекарственным препаратом ингаляционной формы в небулайзерах осуществляется различными способами, что определяет возможность их применения в различных клинических ситуациях. Различают 3 основных типа небулайзеров: компрессорные, ультразвуковые и мэш-небулайзеры. В компрессорных небулайзерах образование аэрозоля достигается за счет подачи мощной струи воздуха, в ультразвуковых — за счет колебания пьезоэлектрического кристалла на ультразвуковых частотах. Техническим достижением последних лет являются мэш-небулайзеры. Особенностью их структуры является вибрирующая мембрана или пластина с микроскопическими отверстиями, через которую пропускается жидкая лекарственная субстанция, что приводит к генерации аэрозоля. Данный тип небулайзеров выгодно отличают от предшественников малое время ингаляции, формирование аэрозоля с частицами одинакового размера — 3—5 мкм, портативность, а также отсутствие ограничения по применению различных видов ингаляционных препаратов [21, 22].
Техническим достижением последних лет являются мэш-небулайзеры. Особенностью их структуры является вибрирующая мембрана или пластина с микроскопическими отверстиями, через которую пропускается жидкая лекарственная субстанция, что приводит к генерации аэрозоля. Данный тип небулайзеров выгодно отличают от предшественников малое время ингаляции, формирование аэрозоля с частицами одинакового размера — 3—5 мкм, портативность, а также отсутствие ограничения по применению различных видов ингаляционных препаратов [21, 22].
Говоря о периоперационном ведении больных хроническими стенозами гортани и трахеи, стоит уделить отдельное внимание системной антимикробной профилактике и антибиотикотерапии. Под антимикробной профилактикой понимают очень короткий курс назначения антимикробного препарата непосредственно перед началом операции. Антимикробная профилактика — четко спланированное мероприятие, направленное на снижение интраоперационной микробной контаминации до уровня, не превышающего возможностей защитных сил организма. Ввиду этого препарат для антибиотикопрофилактики должен соответствовать определенным критериям: обладать бактерицидным действием, иметь длительное время полувыведения, быть достаточно устойчивым к развитию резистентности у микроорганизмов, не иметь выраженных токсических эффектов и не повышать риск геморрагий. Также препарат, используемый для антимикробной профилактики, не может иметь слишком широкий спектр действия. Первое введение препарата проводится за 30 мин до операции (вместе с премедикацией). Повторное введение препарата следует осуществлять при длительности операции более 3 ч (за исключением препаратов с периодом полувыведения 6—8 ч или при наличии факторов, увеличивающих время полувыведения), а также при интраоперационной контаминации. Основными препаратами, применяемыми для антимикробной профилактики, являются цефалоспорины первого и второго поколений: цефозалин (в дозировке 1—2 г), цефуроксим (в дозировке 1,5 г), а также амоксициллин/клавуланат (в дозировке 1,2 г) [23].
Ввиду этого препарат для антибиотикопрофилактики должен соответствовать определенным критериям: обладать бактерицидным действием, иметь длительное время полувыведения, быть достаточно устойчивым к развитию резистентности у микроорганизмов, не иметь выраженных токсических эффектов и не повышать риск геморрагий. Также препарат, используемый для антимикробной профилактики, не может иметь слишком широкий спектр действия. Первое введение препарата проводится за 30 мин до операции (вместе с премедикацией). Повторное введение препарата следует осуществлять при длительности операции более 3 ч (за исключением препаратов с периодом полувыведения 6—8 ч или при наличии факторов, увеличивающих время полувыведения), а также при интраоперационной контаминации. Основными препаратами, применяемыми для антимикробной профилактики, являются цефалоспорины первого и второго поколений: цефозалин (в дозировке 1—2 г), цефуроксим (в дозировке 1,5 г), а также амоксициллин/клавуланат (в дозировке 1,2 г) [23].
Для антибактериальной терапии осложнений при реконструктивной хирургии гортани и трахеи на сегодняшний день препаратами выбора являются респираторные фторхинолоны, имеющие высокую активность в отношении основных бактериальных возбудителей. Кроме того, препараты этой группы хорошо проникают в структуру биопленок. По показаниям возможно одномоментное использование второго антибактериального препарата, имеющего более высокую активность в отношении определенных видов возбудителей [24]. Антибиотики группы карбапенемов или ванкомицин назначают только при выраженном активном воспалении в зоне операции и при подтвержденной устойчивости выделенных возбудителей к другим группам антибактериальных препаратов [2].
Кроме того, препараты этой группы хорошо проникают в структуру биопленок. По показаниям возможно одномоментное использование второго антибактериального препарата, имеющего более высокую активность в отношении определенных видов возбудителей [24]. Антибиотики группы карбапенемов или ванкомицин назначают только при выраженном активном воспалении в зоне операции и при подтвержденной устойчивости выделенных возбудителей к другим группам антибактериальных препаратов [2].
Таким образом, существует множество методов по профилактике и лечению осложнений при реконструктивных вмешательствах у пациентов с хроническими стенозами гортани и трахеи. Существующие методики не являются универсальными, поэтому подбор необходимой терапии зависит от многих факторов, включая анамнестические данные, этиологию, индивидуальный характер течения патологического процесса, общесоматический статус пациента.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.
Сведения об авторах
Крюков А.И. — e-mail: [email protected]; https://orcid.org/0000-0002-0149-0676
Гуров А.В. — e-mail: [email protected]; https://orcid.org/0000-0001-9811-8397
Кирасирова Е.А. — e-mail: [email protected]; https://orcid.org/0000-0003-4795-4445
Кулабухов Е.В. — е-mail: [email protected]; https://orcid.org/0000-0003-1446-5346
Автор, ответственный за переписку: Гуров А.В. — e-mail: [email protected]
Крюков А.И., Гуров А.В., Кирасирова Е.А., Кулабухов Е.В. Современные методы профилактики и терапии осложнений при реконструктивной хирургии у пациентов со стенозом гортани и трахеи. Вестник оториноларингологии. 2019;84(6):48-53.
Стеноз гортани — подразделение дыхательных путей, обслуживание Оторино -ларингологии
- Дом
- Пациенты и семейства
- Глоссарий
- Стеноз гортани
Стеноз на летном возрасте. . Сужение голосовых связок называется голосовым стенозом , а сужение чуть ниже голосовых связок — подскладочным стенозом . Сужение может быть связано с одним или несколькими уровнями гортани.
. Сужение голосовых связок называется голосовым стенозом , а сужение чуть ниже голосовых связок — подскладочным стенозом . Сужение может быть связано с одним или несколькими уровнями гортани.
Перепонка голосовой щели представляет собой мембрану различной толщины и может включать в себя голосовые связки разной длины. Стеноз задней (задней) части голосовой щели с фиксацией суставов голосовых связок или без нее называется стенозом задней голосовой щели . Сужение, затрагивающее все уровни гортани, называется транссвязочным стенозом.
Ребенок мог родиться с врожденной аномалией перстневидного хряща (врожденный подсвязочный стеноз). У очень недоношенного ребенка может быть предрасположенность к такой патологии. Часто такой младенец интубируется в течение нескольких недель, что приводит к приобретенной форме стеноза (в таком случае смешанная форма: приобретенная по врожденной причине). Врожденный подсвязочный стеноз будет иметь подсвязочный диаметр менее 4,0 мм у доношенного новорожденного и 3,0 мм у недоношенного ребенка.
Случайное удушение, травмы шеи, проглатывание едких продуктов являются некоторыми другими причинами стеноза дыхательных путей. Может быть сопутствующий стеноз глотки и пищевода (пищевода).
Симптомы
При стенозе гортани будут респираторные и голосовые жалобы. Проблемы задней голосовой щели влияют на дыхание. Голосовые жалобы связаны с передней частью голосовой щели. Легкий подсвязочный стеноз может иметь мало симптомов. Умеренное сужение может вызвать шумное дыхание (стридор) и ограничить активность, поскольку у ребенка появляется одышка. У младенцев могут быть проблемы с кормлением. Тяжелый подсвязочный стеноз и слияние голосовых связок требуют введения трахеотомической трубки, чтобы ребенок мог дышать. Голос обычно нормальный, если только стеноз не очень тяжелый или полный.
У детей и младенцев со стенозом подсвязочного пространства могут быть другие связанные проблемы и сопутствующие заболевания, такие как сложные заболевания легких (бронхолегочная дисплазия), сердечные и неврологические состояния, гастроэзофагеальный рефлюкс, проблемы с глотанием и кормлением. Чтобы получить наилучшие результаты при лечении стеноза дыхательных путей, важно, чтобы все сопутствующие проблемы и сопутствующие заболевания лечила многопрофильная команда. Это обеспечит наилучшие условия, прежде чем мы исправим стеноз дыхательных путей. Также может быть несколько синдромов (например, трисомия 21 или синдром Дауна), которые требуют комплексного подхода и особого ухода для достижения оптимальных результатов.
Чтобы получить наилучшие результаты при лечении стеноза дыхательных путей, важно, чтобы все сопутствующие проблемы и сопутствующие заболевания лечила многопрофильная команда. Это обеспечит наилучшие условия, прежде чем мы исправим стеноз дыхательных путей. Также может быть несколько синдромов (например, трисомия 21 или синдром Дауна), которые требуют комплексного подхода и особого ухода для достижения оптимальных результатов.
Уход
Лечение всех видов стеноза гортани. В целом, лечение может быть эндоскопическим или наружным хирургическим. Это решение принимается во время эндоскопической оценки. Иногда может быть несколько уровней стеноза. В таком случае мы никогда не можем думать о деканюляции (удалении трахеостомической канюли), если все уровни не были обработаны оптимально.
Для коррекции подсвязочного стеноза используются две основные операции: ларинготрахеальная реконструкция (LTR) и перстнетрахеальная резекция (CTR). Обе эти операции могут быть выполнены в один или два этапа, и это решение зависит от каждого конкретного случая.
Третьей разновидностью операции является расширенный CTR , который сочетает в себе принципы расширения дыхательных путей с использованием хрящевого трансплантата и перстнетрахеальной резекции.
Следует помнить, что при хирургических вмешательствах на дыхательных путях всегда приходится выбирать между ДЫХАТЕЛЬНЫМИ ПУТЯМИ и ГОЛОСОМ. Приоритет отдается деканюляции (удалению трахеостомической канюли), которая изменяет качество жизни пациента и позволяет избежать многочисленных проблем, связанных с трахеостомией.
Решение о типе операции зависит от точного места стеноза, длины стеноза, вовлечения голосовых связок в стенозированный сегмент и сопутствующих заболеваний.
Комбинированный аэро-пищеварительный стеноз требует поэтапного лечения и включает ЛОР плюс детский или пищеварительный хирург.
Важно отметить, что наилучшие результаты реконструкции дыхательных путей и возможной деканюляции (удаления трахеостомы) достигаются при первой операции.
Рост трахеи нормальный и не изменяется после этих вмешательств. У ребенка нормальное развитие и значительное улучшение качества его жизни.
Последнее обновление: 29 мая 2018 г., 20:00
Что такое стеноз гортани? — Stanford Medicine Children’s Health
Что такое стеноз гортани?
Гортань представляет собой структуру, состоящую из хрящей, мышц и других мягких тканей, расположенную над трахеей и играющую важную роль в способности ребенка дышать, говорить и глотать. Если гортань сужается либо из-за проблемы при рождении, либо из-за травмы, это называется стенозом гортани.
Каковы симптомы стеноза гортани?
Дети со стенозом дыхательных путей могут иметь следующие симптомы:
- Неспособность откашливать выделения
- Сильная одышка
- Шумное дыхание
- Проблемы с едой
- Рецидивирующие крупоподобные инфекции с частотой или в нетипичном возрасте
В других случаях у детей со стенозом дыхательных путей симптомы могут отсутствовать. У недоношенных детей со стенозом дыхательных путей часто диагностируют только после удаления дыхательной трубки, и они не могут адекватно дышать самостоятельно.
У недоношенных детей со стенозом дыхательных путей часто диагностируют только после удаления дыхательной трубки, и они не могут адекватно дышать самостоятельно.
Как диагностируется стеноз гортани?
Диагностика стеноза гортани требует посещения специалиста по уху, горлу и носу или отоларинголога для тщательного медицинского осмотра. У детей, у которых может быть стеноз дыхательных путей, врачи используют микроскоп и камеру для осмотра гортани и трахеи, выявления и измерения сужения дыхательных путей, пока ребенок находится под наркозом в операционной.
Обследование может также включать ларингоскопию в клинике, относительно безболезненную процедуру. Во время ларингоскопии небольшой оптоволоконный эндоскоп вводят через нос и используют для осмотра гортани (голосового ящика). Большинству детей для прохождения процедуры требуется небольшая местная анестезия или ее отсутствие. Пациент и его семья смогут наблюдать за ходом исследования на видеоэкране.
Как лечить стеноз гортани?
Каждый ребенок уникален, поэтому лечение зависит от каждого случая. Лечение стеноза дыхательных путей зависит от локализации и тяжести сужения. При легкой форме лечение может включать только наблюдение. В тяжелых случаях могут потребоваться эндоскопические вмешательства или открытая реконструкция дыхательных путей.
Лечение стеноза дыхательных путей зависит от локализации и тяжести сужения. При легкой форме лечение может включать только наблюдение. В тяжелых случаях могут потребоваться эндоскопические вмешательства или открытая реконструкция дыхательных путей.
Эндоскопические вмешательства
Эндоскопические вмешательства выполняются через рот и не требуют разрезов на коже. Несколько эндоскопических вмешательств были разработаны для лечения детей с обструкцией дыхательных путей. Некоторые из них включают баллонную дилатацию, эндоскопические процедуры расщепления перстневидного хряща и эндоскопические процедуры пластики заднего хряща.
- Баллонная дилатация включает введение специального хирургического баллона в дыхательные пути в месте сужения. Затем баллон надувают, расширяя область сужения. Баллонная дилатация выполняется в операционной под общей анестезией, часто выполняется несколько раз при лечении стеноза дыхательных путей и может использоваться в сочетании с другими процедурами.

- Эндоскопическое расщепление перстневидного хряща включает разрез хрящевого кольца ниже голосовых связок (перстневидное кольцо), что позволяет расширить хрящевое кольцо. Эта процедура проводится в операционной под общим наркозом и может выполняться в сочетании с другими процедурами.
- Эндоскопическая трансплантация заднего хряща включает разрез в задней части хрящевого кольца чуть ниже голосовых связок (перстневидное кольцо) и помещение в разрез кусочка реберного хряща. Эта процедура постоянно расширяет дыхательные пути в этом месте и может выполняться при стенозе гортани или двустороннем параличе голосовых связок. Эта процедура проводится в операционной под общим наркозом.
Открытые вмешательства
Открытые вмешательства выполняются через разрез на шее. Этот разрез обычно очень хорошо заживает и часто может быть включен в трахеостому пациента (отверстие, куда входит трубка), если таковая имеется. Эти открытые хирургические процедуры, предназначенные для лечения стеноза дыхательных путей, часто называют «ларинготрахеопластикой (ЛТП)» или «ларинготрахеальной реконструкцией (ЛТР)» и включают в себя широкий спектр различных методов. Важно помнить, что не все хирургические процедуры подходят для каждого ребенка. Каждая процедура имеет свой собственный набор рисков и преимуществ, и ее следует тщательно выбирать только после всесторонней оценки у детского отоларинголога-хирурга головы и шеи (ЛОР).
Важно помнить, что не все хирургические процедуры подходят для каждого ребенка. Каждая процедура имеет свой собственный набор рисков и преимуществ, и ее следует тщательно выбирать только после всесторонней оценки у детского отоларинголога-хирурга головы и шеи (ЛОР).
Специальные процедуры реконструкции дыхательных путей
Основной целью реконструкции дыхательных путей является расширение области сужения. Существует три основных категории реконструкции дыхательных путей, предназначенных для достижения этой цели:
- Расширяющая ларингопластика: Процедура расширения дыхательных путей и трансплантации, которая включает разрез в передней и/или задней части дыхательных путей, расширение узкого сегмента и размещение ребра хрящей в зоне расширения.
- Резекция трахеи: Процедура, включающая удаление узкой части трахеи и сшивание разрезанных концов нормальной трахеи. Это часто выполняется для сужения трахеи, а не подсвязочного сужения.
 Когда вовлечен подсвязочный аппарат или его компонент, выполняется другая версия резекции трахеи, называемая «крикотрахеальной резекцией (CTR)».
Когда вовлечен подсвязочный аппарат или его компонент, выполняется другая версия резекции трахеи, называемая «крикотрахеальной резекцией (CTR)». - Скользящая трахеопластика: Процедура, включающая разделение трахеи в области сужения с последующим открытием задней и передней части каждого сегмента дыхательных путей в месте стеноза. Затем нижняя часть воздуховода надевается поверх верхней части воздуховода, что позволяет создать более широкий дыхательный путь, когда два сегмента трахеи сшиваются вместе. Когда стеноз находится в верхней половине трахеи, процедура называется «цервикальной» скользящей трахеопластикой. Скользящая трахеопластика также часто выполняется при стенозе трахеи, расположенном дальше по дыхательным путям под грудиной (грудной костью).
Одноэтапная реконструкция дыхательных путей в сравнении с двухэтапной
Реконструкция дыхательных путей часто выполняется у пациентов с наложенной трахеостомой. Одноэтапная процедура относится к технике реконструкции дыхательных путей, которая выполняется одновременно с удалением трахеостомической трубки.

 Причиной такой формы являются инфекционные болезни, травмы гортани после операций и ранений, длительная процедура искусственной вентиляции;
Причиной такой формы являются инфекционные болезни, травмы гортани после операций и ранений, длительная процедура искусственной вентиляции;
 Когда вовлечен подсвязочный аппарат или его компонент, выполняется другая версия резекции трахеи, называемая «крикотрахеальной резекцией (CTR)».
Когда вовлечен подсвязочный аппарат или его компонент, выполняется другая версия резекции трахеи, называемая «крикотрахеальной резекцией (CTR)».