Бактериофаги: препараты. Бактериофаги что это
Что такое бактериофаги?
Бактериофаги или фаги (от др.-греч. φᾰγω – «пожираю») – вирусы, избирательно поражающие бактериальные клетки. Чаще всего бактериофаги размножаются внутри бактерий и вызывают их лизис. Как правило, бактериофаг состоит из белковой оболочки и генетического материала.
История
Английский бактериолог Фредерик Туорт в статье 1915 года описал инфекционную болезнь стафилококков, инфицирующий агент проходил через фильтры, и его можно было переносить от одной колонии к другой. Независимо от Фредерика Туорта французско-канадский микробиолог Феликс Д’Эрелль 3 сентября 1917 года сообщил об открытии бактериофагов. Наряду с этим известно, что российский микробиолог Николай Фёдорович Гамалея ещё в 1897 году впервые наблюдал явление лизиса бактерий (сибиреязвенной палочки) под влиянием перевиваемого агента.
После открытия явлений бактериофагии Д’Эрелль развил учение о том, что бактериофаги патогенных бактерий, являясь их паразитами, играют большую роль в патогенезе инфекций, обеспечивая выздоровление больного организма, а затем создания специфического иммунитета. Это положение привлекло к явлению бактериофагии внимание многих исследователей, которые предполагали найти в фагах важное средство борьбы с наиболее опасными инфекционными болезнями человека и животных. Также Феликс Д’Эрелль выдвинул предположение, что бактериофаги имеют корпускулярную природу. Однако только после изобретения электронного микроскопа удалось увидеть и изучить ультраструктуру фагов.
Бактериофаги в природе
Бактериофаги незримо присутствуют повсюду в нашем мире – в океане, почве, глубоководных источниках, питьевой воде и пище. Они – наиболее представленная форма жизни на Земле – от 1030 до 1032 фаговых частиц в биосфере, – и играют ключевую роль в поддержании баланса всех исследованных экосистем. Бактериофаги являются естественными регуляторами и борцами с бактериями и обеспечивают динамическое равновесие в природе, сохраняя относительное постоянство микробного пейзажа в природе и ограничивая рост популяции бактерий. Бактериофаги присутствуют даже в нашей пище – ежедневное поедание бактериофагов с пищей, в которой они присутствуют естественным образом, регулирует микробный баланс в организме человека.
Знаменитый ученый Д, Эрелль представил миру бактериофаги как естественные антибактериальные агенты и предложил использовать их для терапии – еще до открытия антибиотиков.
Классификация
Различают две группы бактериофагов: умеренные и вирулентные. Умеренные фаги медленно размножаются внутри пораженной бактериальной клетки, передаются внутри бактериальной колонии из поколения в поколение, периодически разрушая микробные клетки. Такой эффект называется лизогенным. Вирулентные фаги, попав в клетку микроба начинают стремительно размножаться, приводя к быстрой гибели зараженной клетки. Такой эффект называется литическим.
Какие проблемы решают препараты бактериофагов?
1.Эффективная борьба с бактериальными инфекциями
Позволяют эффективно бороться с бактериальными инфекциями без риска развития осложнений на печень, почки и другие жизненно важные органы, подвергающиеся повреждающему действию обычных антибактериальных средств.
2.Усиление действия антибиотиков
При совместном применении с антибиотиком могут усиливать эффективность последнего.
3.Уничтожают только вредоносные бактерии
Уничтожают вредоносные бактерии и сохраняют собственные, «полезные» для нас бактерии (кишечную микрофлору, микрофлору половых органов), не вызывая дисбактериоз.
4.Эффективная замена антибиотикам
При отсутствии эффекта от применения антибиотиков (при устойчивости бактерий к антибиотикам) и наличии хронической, рецидивирующей инфекции, бактериофаги являются отличным выбором в качестве препаратов антибактериальной терапии.
5. Минимум противопоказаний
При наличии противопоказаний к применению антибиотиков (при антибиотико ассоциированных диареях, нарушении работы печени и почек и др.) – бактериофаги незаменимы.
6. Бактериофаги могут применяться как внутрь, так и использоваться для наружного применения
Бактериофаги могут применяться как внутрь, так и использоваться для наружного применения, что решает проблему не только на уровне всего организма, но и местно в месте локализации инфекции.
Механизм действия бактериофагов
Вирус проникает в клетку патогенной бактерии, внедряется в ее геном и начинает размножаться. После накопления внутри бактериальной клетки определенного количества новых вирусных частиц (вирионов) клетка разрушается, вирусы выходят наружу и заражают новые бактериальные клетки.
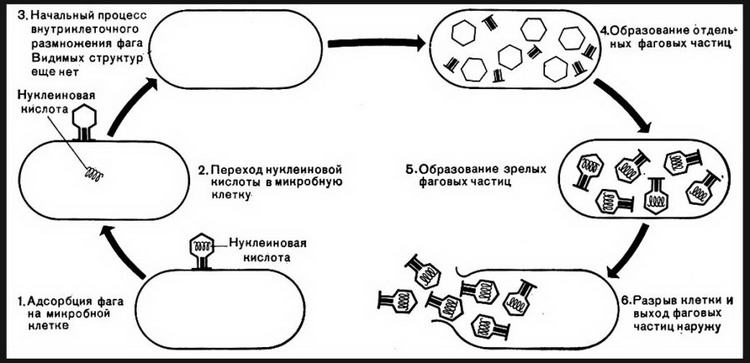
Жизненный цикл бактериофага
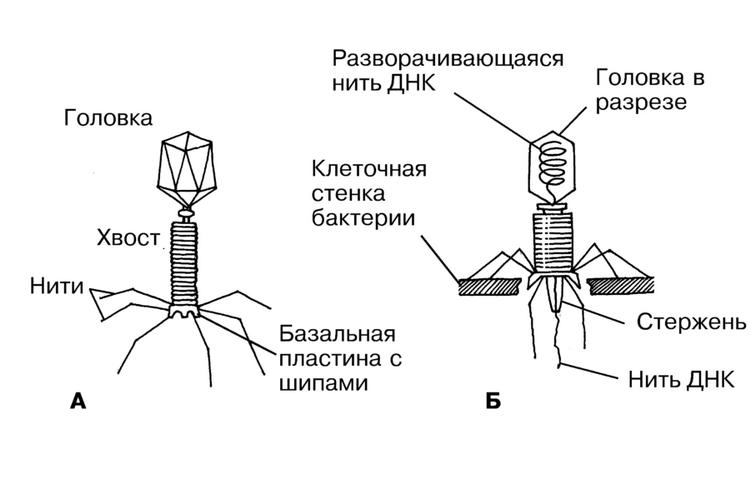
- Фаг приближается к бактерии, и хвостовые нити связываются с рецепторными участками на поверхности бактериальной клетки.
- Хвостовые нити изгибаются и «заякоривают» шипы и базальную пластинку на поверхности клетки; хвостовой чехол сокращается, заставляя полый стержень входить в клетку; этому способствует фермент лизоцим, который находится в базальной пластинке; таким образом, нуклеиновая кислота (ДНК или РНК) вводится внутрь клетки.
- Нуклеиновая кислота фага кодирует синтез ферментов фага, используя для этого белоксинтезирующий аппарат хозяина.
- Фаг тем или иным способом инактивирует ДНК и РНК хозяина, а ферменты фага совсем расщепляют её; РНК фага подчиняет себе клеточный аппарат.
- Нуклеиновая кислота фага реплицируется и кодирует синтез новых белков оболочки.
- Новые частицы фага, образовавшиеся в результате спонтаной самосборки белковой оболочки вокруг фаговой нуклеиновой кислоты; под контролем РНК фага синтезируется лизоцим.
- Лизис клетки: клетка лопается под воздействием лизоцима; высвобождается около 200-1000 новых фагов; фаги инфицируют другие бактерии.
- Стадии 1-7 по времени занимают около 30 минут; этот период называется латентным периодом.
Две стороны медали
Достоинства
Бактерии теряют чувствительность к действию антибиотиков. Фармацевтическая промышленность неустанно синтезирует другие. Однако известно, что возможности синтеза антибиотиков ограничены. К действию бактериофагов антибиотики приспосабливаются очень тяжело, а, как утверждают специалисты, к комплексу из нескольких бактериофагов микробы не могут выработать резистентность и вовсе. Кроме того, бактериофаги практически не имеют побочного действия, реже вызывают аллергические явления, могут сочетаться с любыми препаратами. Бактериофаги в настоящий момент хорошо зарекомендовали себя при лечении урологических заболеваний, гнойных процессов в хирургии, а также при лечении инфекционных заболеваний кишечника у новорожденных детей.
Недостатки
- К сожалению, недостатков у медицинских бактериофагов тоже немало. Самая главная проблема проистекает из достоинства – высокой специфичности фагов. Каждый бактериофаг инфицирует строго определенный тип бактерий, даже не таксономический вид, а ряд более узких разновидностей, штаммов. Условно говоря, как если бы сторожевая собака начинала лаять только на одетых в черные плащи громил двухметрового роста, а на лезущего в дом подростка в шортах никак не реагировала. Поэтому для нынешних фаговых препаратов нередки случаи неэффективного применения. Препарат, сделанный против определенного набора штаммов и прекрасно лечащий стрептококковую ангину в Смоленске, может оказаться бессильным против по всем признакам такой же ангины в Кемерове. Болезнь та же, вызывается тем же микробом, а штаммы стрептококка в разных регионах оказываются различными.
Для максимально эффективного применения бактериофага необходима точная диагностика патогенного микроба, вплоть до штамма. Самый распространенный сейчас метод диагностики – культуральный посев – занимает много времени и требуемой точности не дает. Быстрые методы – типирование с помощью полимеразной цепной реакции или масс-спектрометрии – внедряются медленно из-за дороговизны аппаратуры и более высоких требований к квалификации лаборантов. В идеале подбор фагов-компонентов лекарственного препарата можно было бы делать против инфекции каждого конкретного пациента, но это дорого и на практике неприемлемо.
- Другой важный недостаток фагов – их биологическая природа. Кроме того, что бактериофаги для поддержания инфекционности требуют особых условий хранения и транспортировки, такой метод лечения открывает простор для множества спекуляций на тему «посторонней ДНК в человеке». И хотя известно, что бактериофаг в принципе не может заразить человеческую клетку и внедрить в нее свою ДНК, поменять общественное мнение непросто.
- Из биологической природы и довольно большого, по сравнению с низкомолекулярными лекарствами (теми же антибиотиками), размера вытекает третье ограничение – проблема доставки бактериофага в организм. Если микробная инфекция развивается там, куда бактериофаг можно приложить напрямую в виде капель, спрея или клизмы, – на коже, открытых ранах, ожогах, слизистых оболочках носоглотки, ушей, глаз, толстого кишечника – то проблем не возникает.
- Но если заражение происходит во внутренних органах, ситуация сложнее. Случаи успешного излечения инфекций почек или селезенки при обычном пероральном приеме препарата бактериофага известны. Но сам механизм проникновения относительно крупных (100 нм) фаговых частиц из желудка в кровоток и во внутренние органы изучен плохо и сильно разнится от пациента к пациенту. Бактериофаги бессильны и против тех микробов, которые развиваются внутри клеток, например возбудителей туберкулеза и проказы. Через стенку человеческой клетки бактериофаг пробраться не может.
Нужно отметить, что противопоставлять применение бактериофагов и антибиотиков в медицинских целях не следует. При совместном их действии наблюдается взаимное усиление противобактериального эффекта. Это позволяет, например, снизить дозы антибиотиков до значений, не вызывающих выраженных побочных эффектов. Соответственно, и механизм выработки у бактерий устойчивости к обоим компонентам комбинированного лекарства почти невозможен.
Расширение арсенала противомикробных препаратов дает больше степеней свободы в выборе методики лечения. Таким образом, научно обоснованное развитие концепции применения бактериофагов в противомикробной терапии – перспективное направление. Бактериофаги служат не столько альтернативой, сколько дополнением и усилением в борьбе с инфекциями.
Применение
В медицине
Одной из областей использования бактериофагов является антибактериальная терапия, альтернативная приёму антибиотиков. Например, применяются бактериофаги: стрептококковый, стафилококковый, клебсиеллёзный, дизентерийный поливалентный, пиобактериофаг, коли, протейный и колипротейный и другие. В настоящее время их применяют для лечения бактериальных инфекций, которые не чувствительны к традиционному лечению антибиотиками, особенно в республике Грузия. Обычно, применение бактериофагов сопровождается большим, чем антибиотики, успехом там, где присутствуют биологические мембраны, покрытые полисахаридами, через которые антибиотики обычно не проникают. В настоящее время терапевтическое применение бактериофагов не получило одобрения на Западе, хотя и применяются фаги для уничтожения бактерий, вызывающих пищевые отравления, таких, как листерии. В многолетнем опыте в объёме крупного города и сельской местности доказана необычайно высокая лечебная и профилактическая эффективность дизентерийного бактериофага.
В биологии
Бактериофаги применяются в генной инженерии в качестве векторов, переносящих участки ДНК, возможна также естественная передача генов между бактериями посредством некоторых фагов (трансдукция).
Фаговые векторы обычно создают на базе умеренного бактериофага λ, содержащего двухцепочечную линейную молекулу ДНК. Левое и правое плечи фага имеют все гены, необходимые для литического цикла (репликации, размножения). Средняя часть генома бактериофага λ (содержит гены, контролирующие лизогению, то есть его интеграцию в ДНК бактериальной клетки) не существенна для его размножения и составляет примерно 25 тысяч пар нуклеотидов. Данная часть может быть заменена на чужеродный фрагмент ДНК. Такие модифицированные фаги проходят литический цикл, но лизогения не происходит. Векторы на основе бактериофага λ используют для клонирования фрагментов ДНК эукариот (то есть более крупных генов) размером до 23 тысяч пар нуклеотидов (т. п. н.). Причём, фаги без вставок – менее 38 т. п. н. или, напротив, со слишком большими вставками – более 52 т. п. н. не развиваются и не поражают бактерии.
Поскольку размножение бактериофага возможно только в живых клетках, бактериофаги могут быть использованы для определения жизнеспособности бактерий. Данное направление имеет большие перспективы, поскольку, одним из основных вопросов при разных биотехнологических процессах является определение жизнеспособности используемых культур. С помощью метода электрооптического анализа клеточных суспензий была показана возможность изучения этапов взаимодействия фаг-микробная клетка.
Видео
Источники
mfina.ru
Бактериофаги
Бактериофаги (вирусы бактерий)
Бактериофаги (от «бактерия» и греч. phagos — пожирающий)—вирусы бактерий, специфически проникающие в бактерии, паразитирующие в них вплоть до гибели (лизиса) бактериальной клетки.
Строение бактериофагов изучают с помощью электронной микроскопии образцов, контрастированных напылением металлов или фосфорно-вольфрамовой кислотой.
В зависимости от формы и структурной организации фаги подразделяют на несколько морфологических типов:
нитевидные;
мелкие кубические (некоторые из них имеют аналоги отростков), без отростка, с коротким отростком, с длинным отростком;
фаги сперматозоидной формы, т. е. с кубической головкой и хвостовым отростком, имеющие сокращающийся или не сокращающийся чехол отростка.
Размеры фагов колеблются от 20 до 800 нм (нитевидный тип).
Наиболее изучены крупные бактериофаги, имеющие форму сперматозоида и сокращающийся чехол отростка, например, колифаги Т2, Т4, Т6. Они состоят из головки икосаэдрического типа размером 65—100 нм и хвостового отростка длиной более 100 нм (рис. 3.14).
Хвостовой отросток имеет внутри полый цилиндрический стержень, сообщающийся с головкой, а снаружи — чехол, способный к сокращению, наподобие мышцы. Чехол присоединен к воротничку, окружающему стержень около головки. На дистальном конце отростка имеется шестиугольная базальная ,пластинка с шипами, от которых отходят нитевидные структуры — фибриллы.
Бактериофаги содержат или ДНК, или РНК. Нуклеиновые кислоты фагов могут быть двунитевыми, однонитевыми, линейными, кольцевыми. Большинство фагов содержит двунитевую ДНК, замкнутую в кольцо.
У фагов, имеющих форму сперматозоида, одна молекула двунитевой суперспирализованной ДНК находится внутри головки и защищена капсидом. Капсид состоит из белковых молекул — идентичных полипептидных субъединиц, уложенных по икосаэдрическому (кубическому) типу симметрии. В состав головки также входит полипептид, состоящий из аспарагиновой, глутаминовой кислот и лизина. У некоторых фагов внутри головки находится внутренний гистоноподобный белок, обеспечивающий суперспирализацию ДНК. Сокращающийся чехол хвостового отростка образован также белковыми субъединицами, уложенными по спиральному типу симметрии, содержащими АТФ и ионы Са2+. У некоторых фагов (например, Т2) в дистальной части отростка содержится фермент лизоцим.
Антигенные свойства. Бактериофаги содержат группоспецифические и типоспецифические антигены, обладают иммуногенными свойствами, вызывая синтез специфических антител в организме. Антитела, взаимодействуя с бактериофагами, могут нейтрализовать их литическую активность против бактерий. По типоспецифическим антигенам фаги делят на серотипы.
Резистентность. По сравнению с вирусами человека бактериофаги более устойчивы к факторам окружающей среды. Инактивируются под действием температуры 65-70 °С, УФ-облучения в высоких дозах, ионизирующей радиации, формалина и кислот. Длительно сохраняются при низкой температуре и высушивании.
Взаимодействие фагов с бактериальной клеткой. Бактериофаги инфицируют строго определенные бактерии, взаимодействуя со специфическими рецепторами клетки.
По специфичности взаимодействия различают следующие бактериофаги:
поливалентные, взаимодействующие с родственными видами бактерий;
моновалентные, взаимодействующие с бактериями определенного вида;
типовые, взаимодействующие с отдельными типами (вариантами) бактерий данного вида.
Взаимодействие фагов с бактериями может протекать, как и у других вирусов, по:
продуктивному,
абортивному
интегративному типам.
При продуктивном типе взаимодействия образуется фаговое потомство, бактерии лизируются; при абортивном типе — фаговое потомство не образуется и бактерии сохраняют свою жизнедеятельность; при интегративном типе — геном фага встраивается в хромосому бактерии и сосуществует с ней.
В зависимости от типа взаимодействия различают вирулентные и умеренные бактериофаги.
Вирулентные бактериофаги взаимодействуют с бактерией по продуктивному типу. Проникнув в бактерию, они репродуцируются с образованием 200—300 новых фаговых частиц и вызывают лизис бактерий. Взаимодействие бактериофага с бактерией напоминает взаимодействие вирусов человека с клеткой хозяина. Специфическая адсорбция фагов на бактериальной клетке происходит при наличии комплементарных рецепторов липопротеиновой или липополисахаридной природы в ее клеточной стенке. На бактериях, лишенных клеточной стенки (протопласты, сферопласты), бактериофаги не адсорбируются. Некоторые фаги в качестве рецепторов используют половые пили бактерий.
Фаги, имеющие хвостовой отросток, прикрепляются к бактериальной клетке свободным концом отростка (фибриллами, базальной пластинкой). Проникновение фаговой нуклеиновой кислоты в бактерию наиболее изучено у бактериофагов, имеющих отросток с сокращающимся чехлом. В результате активации АТФ чехол хвостового отростка сокращается, и стержень с помощью лизоцима, растворяющего прилегающий фрагмент клеточной стенки, как бы просверливает оболочку клетки. При этом ДНК фага, содержащаяся в его головке, проходит в форме нити через канал хвостового стержня и инъецируется в клетку, а капсид фага остается снаружи бактерии.
Некоторые мелкие кубические фаги, способные адсорбироваться на половых пилях, вводят свою нуклеиновую кислоту через канал этих пилей. ДНК нитевидных фагов проходит в бактерию вместе с одним из капсид-ных белков.
Инъецированная внутрь бактерии нуклеиновая кислота подавляет биосинтез компонентов клетки, заставляя ее синтезировать нуклеиновую кислоту и белки фага. Эти процессы схожи с репродукцией вирусов человека. После образования компонентов фага происходит самосборка частиц: сначала пустотелые капсиды головок заполняются нуклеиновой кислотой, затем сформированные головки соединяются с хвостовыми отростками. В результате изменения внутриклеточного осмотического давления и действия фагового лизоцима происходит разрушение оболочки, лизис бактерии и выход фагов из нее. Весь литический цикл от адсорбции бактериофага на бактерии до его выхода из нее занимает 20-40 мин.
Умеренные бактериофаги в отличие от вирулентных взаимодействуют с чувствительными бактериями либо по продуктивному, либо по интегративному типу. Продуктивный цикл умеренного фага идет в той же последовательности, что и у вирулентных фагов, и заканчивается лизисом клетки. При интегративном типе взаимодействия ДНК умеренного фага встраивается в хромосому бактерии, реплицируется синхронно с геномом размножающейся бактерии, не вызывая ее лизиса. ДНК бактериофага, встроенная в хромосому бактерии, называется профагом, а культура бактерий — лизогенной. Такое сосуществование бактерии и умеренного бактериофага называется лизогенией (от греч. lysis — разложение, genea — происхождение). Профаг, ставший частью хромосомы бактерии, при ее размножении передается по наследству потомкам.
Каким образом нуклеиновая кислота присоединяется к бактериальной хромосоме?После проникновения в бактерию ДНК умеренного фага приобретает форму кольца, а затем интегрирует по типу кроссинговера в строго определенную гомологичную область хромосомы клетки.
Итак, при лизогении образование фагового потомства не происходит. В основе «сдерживающего» механизма репродукции фагов лежит образование в бактерии специфического репрессора — низкомолекулярного белка, подавляющего транскрипцию фаговых генов. Биосинтез репрессора детерминируется генами профага. Наличием репрессора можно объяснить способность лизогенных бактерий приобретать иммунитет (невосприимчивость) к последующему заражению гомологичным или близкородственными фагами. Под иммунитетом в данном случае понимается такое состояние бактерии, при котором исключается процесс вегетативного размножения вышеуказанных фагов и лизис клетки. Однако термин «лизогения» отражает потенциальную возможность лизиса бактерии, содержащей профаг. Действительно, профаги некоторой части лизогенной культуры бактерий могут спонтанно (самопроизвольно) или направленно под действием ряда физических или химических факторов дерепрессироваться, исключаться из хромосомы, переходить в вегетативное состояние. Этот процесс заканчивается продукцией фагов и лизисом бактерий. Частота спонтанного лизиса бактерий в лизогенных культурах невелика (102, 10~6), т. е. не захватывает все клетки, обладающие иммунитетом. Частоту лизиса бактерий можно значительно увеличить, воздействуя на лизогенную культуру индуцирующими агентами (УФ-лучи, ионизирующее излучение, перекисные соединения, митомицин С и др.). Сам же феномен воздействия, приводящий к инактивации репрессора, называется индукцией профага. Явление индукции используют в генной инженерии. Однако спонтанный лизис лизогенных культур может нанести вред микробиологическому производству. Так, если микроорганизмы — продуценты биологически активных веществ оказываются лизогенными, существует опасность перехода фага в вегетативное состояние, что приведет к лизису производственного штамма этого микроба.
Геном профага может придавать бактерии новые, ранее отсутствовавшие у нее свойства. Этот феномен изменения свойств микроорганизмов под влиянием профага получил название фаговой конверсии (от лат. conver-sio— превращение). Конвертироваться могут морфологические, культуральные, биохимические, антигенные и другие свойства бактерий. Например, наличие профага в дифтерийной палочке обусловливает ее способность продуцировать дифтерийный экзотоксин.
Умеренные фаги могут быть дефектными, т. е. неспособными образовывать зрелые фаговые частицы ни в естественных условиях, ни при индукции. Геном некоторых умеренных фагов (Р1) может находиться в цитоплазме бактериальной клетки в так называемой плаз-мидной форме, не включаясь в ее хромосому. Такого рода умеренные фаги используют в качестве векторов в генной инженерии.
Практическое применение фагов. Бактериофаги используют в лабораторной диагностике инфекций при внутривидовой идентификации бактерий, т. е. определении фаговара (фаготипа). Для этого применяют метод фаготипирования, основанный на строгой специфичности действия фагов: на чашку с плотной питательной средой, засеянной «газоном» чистой культурой возбудителя, наносят капли различных диагностических типоспецифических фагов. Фаговар бактерии определяется тем типом фага, который вызвал ее лизис (образование стерильного пятна, «бляшки», или «негативной колонии», фага). Методику фаготипирования используют для выявления источника и путей распространения инфекции (эпидемиологическое маркирование). Выделение бактерий одного фаговара от разных больных указывает на общий источник их заражения.
По содержанию бактериофагов в объектах окружающей среды (например, в воде) можно судить о присутствии в них соответствующих патогенных бактерий. Подобные исследования проводят при эпидемиологическом анализе вспышек инфекционных болезней.
Фаги применяют также для лечения и профилактики ряда бактериальных инфекций. Производят брюшнотифозный, сальмонел-лезный, дизентерийный, синегнойный, стафилококковый, стрептококковый фаги и комбинированные препараты (колипротейный, пиобактериофаги и др). Бактериофаги назначают по показаниям перорально, парентерально или местно в виде жидких, таблетированных форм, свечей или аэрозолей.
Бактериофаги широко применяют в генной инженерии в качестве векторов для получения рекомбинантных ДНК.
Качественный метод определения фагов E.coli. Чашку Петри с питательным агаром засевают суточной бульонной культурой кишечной палочки газоном и подсушивают при 37 "С в течение 10—15 мин. Затем на поверхность газона наносят каплю фага и наклоняют так, чтобы капля стекла к противоположному краю. После суточной инкубации в термостате просматривают чашку, отмечая наличие зоны лизиса по месту стекания капли фага.
Количественный метод — определение титра фага по методу Грациа. Для постановки опыта предварительно: а) разливают питательный агар в чашки Петри, подсушивают в термостате; б) приготовленный полужидкий (0,7 %) питательный агар, разлитый по 3—4 мл в пробирки, растапливают в водяной бане. Делают 10-кратные разведения исследуемого фага (10~2—10~7 в зависимости от предполагаемого титра) в изотоническом растворе хлорида натрия. Затем 0,5 мл из последнего разведения фага (10~7) смешивают с таким же объемом суточной бульонной культуры чувствительных к фагу бактерий и выливают в пробирку с полужидким агаром, охлажденным до 45 "С. Смесь быстро выливают на поверхность агара в чашке Петри, где она застывает в виде тонкого слоя. Так же готовят смесь из следующего разведения фага (10~6) с бактериями и полужидким агаром и выливают на поверхность агара в другой чашке, затем — из разведения 10~5. После застывания второго слоя агара чашки инкубируют при 37 *С, затем подсчитывают число негативных колоний фага. Число этих колоний соответствует количеству фаговых частиц в засеянной смеси. Исходя из него, можно вычислить количество пятнообразующих единиц в 1 мл исходной суспензии фага. Эта величина, характеризующая концентрацию фага, называется его титром (табл. 5.3.1).
Определение спектра литического действия фага. Чашку с питательным агаром делят на квадраты по числу испытуемых бактериальных культур. На каждый квадрат петлей наносят каплю соответствующей бульонной культуры и распределяют ее по агару в пределах данного квадрата. Затем на каждый засеянный квадрат петлей или пастеровской пипеткой наносят по одной капле испытуемого фага. После суточной инкубации в термостате просматривают чашку, отмечая те квадраты, где имеется сплошной лизис бактерий или так называемые стерильные пятна набактериальном газоне. Количество различных бактериальных культур, которые лизируются испытуемым фагом, определяет широту спектра его литического действия.
Фаготипирование бактерий. Испытуемую суточную бульонную культуру бактерий засевают на поверхность питательного агара в чашке Петри, слегка подсушивают в термостате, затем делят на квадраты, на которые пастеровской пипеткой наносят по одной капле различных типоспецифических фагов. После суточной инкубации отмечают на чашке те квадраты, в которых имеется сплошной лизис бактерий. Фаготип бактериальной культуры определяется тем типом фага, который вызывает ее лизис.
Определение лизогении. Исследуемую суточную бульонную культуру центрифугируют для отделения фага от бактерий. В том случае, если бактерии спонтанно продуцируют фаг, последний будет содержаться в надосадочной жидкости. Для выявления фага надосадочную жидкость засевают на газон индикаторной (чувствительной) бактериальной культуры, на котором через
1 сут инкубации при 37 "С образуются очаги лизиса — "стерильные" пятна. При отрицательном результате опыта исследуемую бактериальную культуру предварительно подвергают УФ-облучению с целью индукции содержащегося в ней профага. Затем поступают так же, как и в предыдущем опыте.
8
studfiles.net
Бактериофаги: виды и назначение
Фаголизис – процесс разрушения фагами бактерий, обычно происходит в пораженном органе при спонтанном выздоровлении. В случае, если самовыздоровление не наступило, организму можно помочь введением соответствующего бактериофага, полученного в условиях фармацевтического предприятия. Бактериофагами называют вирусы бактерий, которые при встрече с чувствительными к ним микробными клетками проникают внутрь и вызывают их растворение (лизис).
В переводе с греческого бактериофаг означает «пожиратель бактерий». В природе эти микроорганизмы весьма разнообразны и составляют самую крупную из известных на сегодняшний день групп вирусов. Фаги имеют отличное от вирусов растений, животных и человека строение, более сложное. Они встречаются в атмосферных осадках, в воздухе, в почве, в еде, на предметах, коже, шерсти животных, словом, везде, где встречаются бактерии.
В последние годы возрастает интерес к бактериофагам, применяемым в качестве альтернативы антибиотикам. И это неудивительно, и те и другие препараты непосредственно влияют на возбудителей инфекций. Однако антибиотики, как известно, губительно действуют не только на патогенную флору, но и на полезную. Бактериофаги, виды которых различны, действуют избирательно, только на «свою» бактерию, оставляя от нее обломки. Собственно, поэтому ученые и не стали придумывать им названия, ведь проще называть их соответственно бактериям, на которые они воздействуют.
Бактериофаги: виды
Выпускают стрептококковый, коли-протейный, клебсиеллезный, стафилококковый, синегнойный, сальмонеллезный, дизентерийный, брюшнотифозный бактериофаги, а также «Интестифаг» и «Пиобактериофаг».
Активность препаратов определяется степенью их разведения, при которой происходит лизис чувствительной культуры. Так, титр 10 в 6-ой степени означает, что данный бактериофаг проявляет литические свойства при разведении в 1 000 000 раз. При температуре 4-6 С препараты сохраняют свои свойства до 12 лет.
В зависимости от формы выпуска различаются и активностью бактериофаги. Виды препаратов позволяют воздействовать как на отдельных возбудителей, так и на несколько сразу. Монофаги воздействуют на несколько штаммов одной бактерии. К комплексным препаратам (поливалентным) относят бактериофаг «Секстафаг», который одновременно способен подавлять активность стафилококков, стрептококков, включая энтерококки, синегнойной и кишечной палочки, протея, клебсиеллы. Кроме того, существует «Интестифаг», предназначенный для лечения кишечных инфекций, он включает сальмонеллезный, брюшнотифозный, дизентерийный, протейный, коли и стрептококковый (подавляющий энтерококки) фаги.
Используют препараты при дисбактериозах, кишечных инфекциях, воспалительных процессах мочеполовой системы и бронхо-легочного аппарата, для лечения гнойно-септических процессов, а также при заболеваниях полости рта и пазух носа. Их применяют как внутрь, в том числе и в виде клизм, так и местно – для полосканий, промываний ран, спринцеваний. К примеру, «Бактериофаг клебсиелл поливалентный очищенный», предназначенный для лечения озены, риносклеромы, инфекций, вызванных бактерией клебсиелла пневмония, применяют ингаляционно при поражениях трахеи, гортани и глотки, вводят турунду, смоченную в жидкости, при отитах, используют для промываний при синуситах. При циститах, энтероколитах, уретритах, пневмониях препарат принимают внутрь.
Бактериофаги обладают массой преимуществ перед антибиотиками. Они не имеют побочных действий, их назначают даже новорожденным и беременным женщинам, они не вызывают привыкания. Их можно сочетать с любыми лекарственными средствами, а также использовать для профилактики инфекционных болезней. Эти препараты оказывают благотворное влияние на становление иммунитета, не подавляют естественную флору, их действие проявляется в течение 2-4 часов после приема. К ним не развивается резистентность патогенных микроорганизмов.
Один недостаток имеют бактериофаги. Виды их, используемые сегодня в медицине, пока немногочисленны, что ограничивает их применение при многих инфекциях.
Перспективы применения
Для того чтобы успешно применять биопрепараты, необходимо определять чувствительность к ним бактерий. Однако ученые заметили интересную закономерность: чувствительность микроорганизмов к фагам не снижается, а наоборот, возрастает, что объясняют обогащением препаратов новыми культурами. На сегодняшний день бактериофаг стафилококковый успешно лизирует до 90% всех штаммов этих бактерий, выделяемых при гнойно-септических поражениях.
Многие инфекционисты полагают, что фаготерапия вскоре совершит революцию в борьбе с заболеваниями. Иммунологи видят перспективу использования этих средств там, где бессильны иммунопрепараты. Согласно данным аналитических исследований, в ближайшие несколько лет одним из самых перспективных направлений фармакологии станет производство фагов.
fb.ru
Бактериофаги | Метки: это, фаг
Бактериофаги это вирусы, избирательно поражающие бактериальные клетки. Бактериофаги размножаются в бактериях и вызывают их растворение. Как правило бактериофаг состоит из белковой оболочки и генетического материала – одноцепочечной или двуцепочечной РНК. Размер частиц приблизительно от 20 до 200 нанометров.
Жизненный цикл бактериофага
- Фаг приближается к бактерии, и хвостовые нити связываются с рецепторными участками на поверхности бактериальной клетки.
- Хвостовые нити изгибаются и «заякоривают» шипы и базальную пластинку на поверхности клетки; хвостовой чехол сокращается, заставляя полый стержень входить в клетку; этому способствует фермент лизоцим, который находится в базальной пластинке; таким образом нуклеиновая кислота (ДНК или РНК) вводится внутрь клетки.
- Нуклеиновая кислота фага кодирует синтез ферментов фага, используя для этого белоксинтезирующий аппарат хозяина.
- Фаг тем или иным способом инактивирует ДНК и РНК хозяина, а ферменты фага совсем расщепляют её; РНК фага подчиняет себе клеточный аппарат.
- Нуклеиновая кислота фага реплицируется и кодирует синтез новых белков оболочки.
- Новые частицы фага, образовавшиеся в результате спонтаной самосборки белковой оболочки вокруг фаговой нуклеиновой кислоты; под контролем РНК фага синтезируется лизоцим.
- Лизис клетки: клетка лопается под воздействием лизоцима; высвобождается около 200-1000 новых фагов; фаги инфицируют другие бактерии.
- Стадии 1-7 по времени занимают около 30 минут; этот период называется латентным периодом.
Лечение бактериофагами
Бактериофаги используют для антибактериальной терапии, альтернативно приёму антибиотиков.
Очень важным свойством бактериофагов является их специфичность: бактериофаги лизируют культуры определенного вида, более того, существуют так наз. типовые бактериофаги, лизирующие варианты внутри вида.
Выявить бактериофаги можно путем нанесения содержащего бактериофаг материала на плотные питательные среды, засеянные газоном чувствительной бактериальной культуры. В том месте газона, куда попал бактериофаг, образуется стерильное пятно или бляшка – зона лизиса бактерий газона вследствие размножения бактериофага. Количество образовавшихся негативных колоний бактериофага соответствует количеству бактериофагов в материале.
Бактериофаги применяют для профилактики и лечения некоторых бактериальных инфекций. В последнее время интерес к ним возрос в связи с широким распространением лекарственно-устойчивых форм патогенных и условно-патогенных бактерий. Препараты бактериофагов выпускают в виде таблеток, мазей, аэрозолей, свечей, в жидком виде. Употребляют их для орошения, смазывания раневых поверхностей, вводят перорально, внутривенно и т.д.
У каждого обитателя Вселенной свое назначение: все в природе гармонично и взаимосвязано, все имеет свои логические связи и требует баланса, чтобы жить в равновесии и гармонии
Бактериофаги -(отбактериии греч.fagos – пожиратель) – это особые представители царства вирусов.
Особенность бактериофагов в том, что они приспособились использовать для своего размножения клетки бактерий.
Эти маленькие создания потрясающе многообразны.
Вирусы бактериий, иначе называемые бактериофагами, – крупнейшая из известных групп вирусов.
Современная классификация бактериофагов включает 13 семейств, подразделенных более чем на 140 родов, которые содержат более 5300 видов фагов.
Применение современных электронных микроскопов позволило детально изучить строение фагов. Оказалось, что многие из них устроены сложнее, чем вирусы человека, животных и растений.
Как выглядят бактериофагии?
Они очень маленькие, самые мелкие – не имеют и клеточки. Размер фага 0,1-0,2 миллимикрона (миллионные доли миллиметра!), что примерно составляет 1/1000 часть от бактериальной клетки величиной около 5 микрон.
Выглядят фаги необычно. Есть среди них и такие, что похожи на маленькие космические станции: аккуратные кристаллы с четкими гранями, стоящие на ножках-фибриллах. Стенки «корпуса» кристалла выстроены из молекул белка, а внутри конструкции находится генная информация фага – ДНК или РНК
Где живут бактериофаги «на воле»?
У них очень разная морфология, и среда обитания. Они живут везде, где есть бактерии – в воде, в почве, в каплях дождя, на поверхностях предметов, овощей, фруктов, на шерсти животных, на коже человека и внутри организма.
Чем богаче среда микроорганизмами, тем больше в ней фагов. Особенно много фагов в черноземе и почвах, в которые вносились органические удобрения. В 1 мм3 обыкновенной воды – около миллиарда фагов.
Человек и Бактериофаг
Человек уже не пьет сырую воду из рек, не моется в естественных водоемах. Когда вода попадает в водопровод, то она обязательно проходит жесткую систему обработки хлорирования. И, фактически, все живые существа, которые живут в воде, гибнут.
Да, мы избавляемся от очень многих вредных микробов, но, к сожалению, мы избавляемся и от наших микро друзей.
Почему так страшно использовать антибиотики, когда они не показаны, когда человек еще не настолько болен, что ему нужны такие радикальные мощные средства? Потому что антибиотики затрагивают всю популяцию бактерий и нормофлору.
Бактериофаги – естественные ограничители популяции бактерий.
Каждый бактериофаг проникает в «свою» бактерию путем специального механизма и начинает там размножаться. Размножается он там до тех пор, пока не разорвет бактерию и не выйдет наружу. И тогда уже много бактериофагов начинают искать себе бактерии для того, чтобы в ней воспроизвестись.
От бактерии остаются лишь обломки, зато на свет появляются не менее 100-200 новых фагов, готовых к нападению. Цикл – время с момента заражения бактерии до выхода потомства – длится всего от 15 до 40 минут в зависимости от вида фага.
Фаги строго избирательны.
Ученые даже не стали присваивать фагам имена: гораздо удобнее называть фага по имени бактерии. Есть фаги стрептококковые, фаги дизентерийные, фаги стафилококковые и т.д., они существуют благодаря бактериям. Где есть бактерии, там есть и фаги: в почве, воде ручья, озера, внутри организма и на коже человека, животного.
В микромире фаги играют роль естественных ограничителей численности бактерий. Количество фагов колеблется в зависимости от количества бактерий.
Если количество нужных фагу бактерий снижается, то и фагов становится меньше, иначе им негде будет размножаться. Поэтому фаги ограничивают, но не уничтожают полностью популяцию бактерий.
Соотношение фагов и соответствующих бактерий находится в таком же балансе, как и соотношение хищников и грызунов в макромире.
Что говорят специалисты.
Прогноз инфекционистов: «Фаготерапия в скором времени станет прорывом в борьбе с инфекциями.
Прогноз иммунологов: «Фаготерапия займет ту нишу, где несостоятельна современная иммунотерапия»
Прогноз аналитиков :«В течение пяти лет производство бактериофагов станет одной из лидирующих отраслей в фармацевтической промышленности»
История бактериофагов.
1896 год -открытие бактериофагов Британским бактериологом Эрнестом Ханкин 1898 год – бактериофаги исследованы российским ученым Николаем Гамалея.В этом же году фаги стали использовать при лечении ран и различных инфекций. 1920-е годы – Феликс д'Эрель – канадский сотрудник Института Пастера (Париж) назвал бактериофаги «бактериофагами» и охарактеризовал их: «вирусы, размножающиеся в бактериях».1940-е годы. Везде, кроме СССР разработки бактериофагов вычеркнуты из числа перспективных исследований. В СССР исследования продолжаются
Во всем мире популярность приобретает метод применения антибиотиков.
1980-е годы Эффективность лечения антибиотиками значительно понизилась Бактерии выработали лекарственную устойчивость.
Интерес к фаговой терапии возобновился
Начало 2000-х годов – Гленн Моррис – сотрудник Университета Мэриленд (США) совместно с НИИ бактериофагов, микробиологии и вирусологии в Тбилиси наладил испытания фаговых препаратов для получения лицензии на их применение в США. Июль 2007 года - бактериофаги одобрены для использования в США На протяжении последних нескольких лет исследования свойств бактериофагов проводятся в России, Грузии, Польше, Франции, Германии, Финляндии, Канаде, США, Великобритании, Мексике, Израиле, Индии, Австралии.Изучение свойств фагов способствовало развитию концепции фаготерапии.
Преимущества Бактериофагов
- действуют лишь на определенные бактерии,
- не нарушают баланса высшего организма,
- постоянно эволюционируют,
- не вызывают побочных эффектов,
- не ослабляют иммунитет,
- не развивают устойчивость бактерий
Альтернатива антибиотикам
- бактериофаги способны уничтожать бактерии, устойчивые к антибиотикам,
- усложняют выработку бактерией механизма устойчивости,
- хорошо проникают в ткани организма человека и животного,
- не подавляют рост нормофлоры,
- не вызывают побочных эффектов,
- сочетаются с любыми лекарственными
- препаратами, оказывают иммуностимулирующее действие.
В Ветеринарии
Профилактика и лечение бактериальных заболеваний птиц и животных- Лечение гнойно-воспалительных заболеваний слизистых глаз, полости рта
- Профилактика гнойно-воспалительных осложнений при ожогах, ранениях, операционных вмешательствах
В Генной инженерии
Фаги- это идеальный объект для генетических манипуляций.- для трансдукции- естественной передачи генов между бактериями
- как векторы, переносящие участки ДНК
В Пищевой промышленности
- В массовом порядке фагосодержащими средствами уже обрабатывают готовые к употреблению продукты из мяса и домашней птицы.
- В разработке – фаговый раствор для распыления на мясе и мясной продукции в убойных цехах.
- Бактериофаги применяют в производстве продуктов питания из мяса, мяса птицы, сыров, растительной продукции, и пр.
В Сельском хозяйстве
- Распыление фагопрепаратов для защиты растений и урожая от гниения и бактериальных заболеваний
- Применение фагопрепаратов для защиты скота иптицы от инфекций и бактериальных заболеваний
Для Экологической безопасности
- антибактериальная обработка семян и растений
- очистка помещений пищеперерабатывающих предприятий
- санитарная обработка рабочего пространства и оборудования
- профилактика помещений больниц
- проведение экологических мероприятий
www.baby.ru
Бактериофаги - это... Что такое Бактериофаги?
Бактериофа́ги (фаги) (от др.-греч. φᾰγω — «пожираю») — вирусы, избирательно поражающие бактериальные клетки. Чаще всего бактериофаги размножаются внутри бактерий и вызывают их лизис. Как правило, бактериофаг состоит из белковой оболочки и генетического материала одноцепочечной или двуцепочечной нуклеиновой кислоты (ДНК или, реже, РНК). Размер частиц приблизительно от 20 до 200 нм.
История
Английский бактериолог Туорт, Фредерик в статье 1915 года описал инфекционную болезнь стафилококков, инфицирующий агент проходил через фильтры, и его можно было переносить от одной колонии к другой.
Независимо от Фредерика Туорта французско-канадский микробиолог Д’Эрель, Феликс 3 сентября 1917 год сообщил об открытии бактериофагов. Наряду с этим известно, что российский микробиолог Николай Фёдорович Гамалея ещё в 1898 году, впервые наблюдал явление лизиса бактерий (сибиреязвенной палочки) под влиянием перевиваемого агента[1][2].
После открытия явлений бактериофагии Д’Эрелль развил учение о том, что бактериофаги патогенных бактерий, являясь их паразитами, играют большую роль в патогенезе инфекций, обеспечивая выздоровление больного организма, а затем создания специфического иммунитета. Это положение привлекло к явлению бактериофагии внимание многих исследователей, которые предполагали найти в фагах важное средство борьбы с наиболее опасными инфекционными болезнями человека и животных.
Также Феликс Д’Эрель выдвинул предположение, что бактериофаги имеют корпускулярную природу. Однако только после изобретения электронного микроскопа удалось увидеть и изучить ультраструктуру фагов. Долгое время представления о морфологии и основных особенностях фагов основывались на результатах изучения фагов Т-группы — Т1, Т2,…, Т7, которые размножаются на Е. coli штамма B. Однако с каждым годом появлялись новые данные, касающиеся морфологии и структуры разнообразных фагов, что обусловило необходимость их морфологической классификации.
Роль бактериофагов в биосфере
Бактериофаги представляют собой наиболее многочисленную, широко распространенную в биосфере и, предположительно, наиболее эволюционно древнюю группу вирусов[3][4]. Приблизительный размер популяции фагов составляет более 1030 фаговых частиц[5].
В природных условиях фаги встречаются в тех местах, где есть чувствительные к ним бактерии. Чем богаче тот или иной субстрат (почва, выделения человека и животных, вода и т. д.) микроорганизмами, тем в большем количестве в нём встречаются соответствующие фаги. Так, фаги, лизирующие клетки всех видов почвенных микроорганизмов, находятся в почвах. Особенно богаты фагами черноземы и почвы, в которые вносились органические удобрения.
Бактериофаги выполняют важную роль в контроле численности микробных популяций, в автолизе стареющих клеток, в переносе бактериальных генов, выступая в качестве векторных «систем»[6].
Действительно, бактериофаги представляют собой один из основных подвижных генетических элементов. Посредством трансдукции они привносят в бактериальный геном новые гены. Было подсчитано, что за 1 секунду могут быть инфицированы 1024 бактерий[7]. Это означает, что постоянный перенос генетического материала распределяется между бактериями, обитающими в сходных условиях.
Высокий уровень специализации, долгосрочное существование, способность быстро репродуцироваться в соответствующем хозяине способствует их сохранению в динамичном балансе среди широкого разнообразия видов бактерий в любой природной экосистеме. Когда подходящий хозяин отсутствует, многие фаги могут сохранять способность к инфицированию на протяжении десятилетий, если не будут уничтожены экстремальными веществами либо условиями внешней среды[8].
Строение бактериофагов
1 — головка, 2 — хвост, 3 — нуклеиновая кислота, 4 — капсид, 5 — «воротничок», 6 — белковый чехол хвоста, 7 — фибрилла хвоста, 8 — шипы, 9 — базальная пластинкаБактериофаги различаются по химической структуре, типу нуклеиновой кислоты, морфологии и характеру взаимодействия с бактериями. По размеру бактериальные вирусы в сотни и тысячи раз меньше микробных клеток.
Типичная фаговая частица (вирион) состоит из головки и хвоста. Длина хвоста обычно в 2 — 4 раза больше диаметра головки. В головке содержится генетический материал — одноцепочечная или двуцепочечная РНК или ДНК с ферментом транскриптазой в неактивном состоянии, окруженная белковой или липопротеиновой оболочкой — капсидом, сохраняющим геном вне клетки[9].
Нуклеиновая кислота и капсид вместе составляют нуклеокапсид. Бактериофаги могут иметь икосаэдральный капсид, собранный из множества копий одного или двух специфичных белков. Обычно углы состоят из пентамеров белка, а опора каждой стороны из гексамеров того же или сходного белка. Более того, фаги по форме могут быть сферические, лимоновидные или плеоморфные[10]. Хвост представляет собой белковую трубку — продолжение белковой оболочки головки, в основании хвоста имеется АТФаза, которая регенерирует энергию для инъекции генетического материала. Существуют также бактериофаги с коротким отростком, не имеющие отростка и нитевидные[11].
Фаги, как и все вирусы, являются абсолютными внутриклеточными паразитами. Хотя они переносят всю информацию для запуска собственной репродукции в соответствующем хозяине, у них отсутствуют механизмы для выработки энергии и рибосомы для синтеза белка. У некоторых фагов в геноме содержится несколько тысяч оснований, тогда как фаг G, самый крупный из секвенированных фагов, содержит 480 000 пар оснований — вдвое больше среднего значения для бактерий, хотя всё же недостаточного количества генов для важнейшего бактериального органоида как рибосомы.
Систематика бактериофагов
Большое количество выделенных и изученных бактериофагов определяет необходимость их систематизации. Классификация вирусов бактерий претерпевала изменения: основывалась на характеристике хозяина вируса, учитывались серологические, морфологические свойства, а затем строение и физико-химический состав вириона[12].
В настоящее время согласно Международной классификации и номенклатуре вирусов бактериофаги, в зависимости от типа нуклеиновой кислоты разделяют на ДНК- и РНК- содержащие.
По морфологическим характеристикам ДНК-содержащие фаги выделены в следующие семейства: Myoviridae, Siphoviridae, Podoviridae, Lipothrixviridae, Plasmaviridae, Corticoviridae, Fuselloviridae, Tectiviridae, Microviridae, Inoviridae Plectovirus и Inoviridae Inovirus.
РНК-содержащие: Cystoviridae, Leviviridae[13].
Взаимодействие бактериофага с бактериальными клетками
Адсорбция бактериофагов на поверхности бактериальной клеткиПо характеру взаимодействия бактериофага с бактериальной клеткой различают вирулентные и умеренные фаги[11]. Вирулентные фаги могут только увеличиваться в количестве посредством литического цикла[8]. Процесс взаимодействия вирулентного бактериофага с клеткой складывается из нескольких стадий: адсорбции бактериофага на клетке, проникновения в клетку, биосинтеза компонентов фага и их сборки, выхода бактериофагов из клетки[7][14].
Первоначально бактериофаги прикрепляются к фагоспецифическим рецепторам на поверхности бактериальной клетки. Хвост фага с помощью ферментов, находящихся на его конце (в основном лизоцима), локально растворяет оболочку клетки, сокращается и содержащаяся в головке ДНК инъецируется в клетку, при этом белковая оболочка бактериофага остается снаружи. Инъецированная ДНК вызывает полную перестройку метаболизма клетки: прекращается синтез бактериальной ДНК, РНК и белков. ДНК бактериофага начинает транскрибироваться с помощью собственного фермента транскриптазы, который после попадания в бактериальную клетку активируется. Синтезируются сначала ранние, а затем поздние иРНК, которые поступают на рибосомы клетки-хозяина, где синтезируются ранние (ДНК-полимеразы, нуклеазы) и поздние (белки капсида и хвостового отростка, ферменты лизоцим, АТФаза и транскриптаза) белки бактериофага. Репликация ДНК бактериофага происходит по полуконсервативному механизму и осуществляется с участием собственных ДНК-полимераз. После синтеза поздних белков и завершения репликации ДНК наступает заключительный процесс — созревание фаговых частиц или соединение фаговой ДНК с белком оболочки и образование зрелых инфекционных фаговых частиц[15].
Продолжительность этого процесса может составлять от нескольких минут до нескольких часов[8]. Затем происходит лизис клетки, и освобождаются новые зрелые бактериофаги[11]. Иногда фаг инициирует лизирующий цикл, что приводит к лизису клетки и освобождению новых фагов. В качестве альтернативы фаг может инициировать лизогенный цикл, при котором он вместо репликации обратимо взаимодействует с генетической системой клетки-хозяина, интегрируясь в хромосому или сохраняясь в виде плазмиды[8]. Таким образом, вирусный геном реплицируется синхронно с ДНК хозяина и делением клетки, а подобное состояние фага называется профагом. Бактерия, содержащая профаг, становится лизогенной до тех пор, пока при определенных условиях или спонтанно профаг не будет стимулирован на осуществление лизирующего цикла репликации. Переход от лизогении к лизису называется лизогенной индукцией или индукцией профага. На индукцию фага оказывает сильное воздействие состояние клетки хозяина предшествующее индукции, также как наличие питательных веществ и другие условия, имеющие место в момент индукции. Скудные условия для роста способствуют лизогенному пути, тогда как хорошие условия способствуют лизирующей реакции[8][11][15].
Очень важным свойством бактериофагов является их специфичность: бактериофаги лизируют культуры определенного вида, более того, существуют так называемые типовые бактериофаги, лизирующие варианты внутри вида, хотя встречаются поливалентные бактериофаги, которые паразитируют в бактериях разных видов[16][17].
Жизненный цикл
Умеренные и вирулентные бактериофаги на начальных этапах взаимодействия с бактериальной клеткой имеют одинаковый цикл.
- Адсорбция бактериофага на фагоспецифических рецепторах клетки.
- Инъекция фаговой нуклеиновой кислоты в клетку хозяина.
- Совместная репликация фаговой и бактериальной нуклеиновой кислоты.
- Деление клетки.
- Далее бактериофаг может развиваться по двум моделям: лизогенный либо литический путь. Умеренные бактериофаги после деления клетки находятся в состоянии профага (Лизогенный путь). Вирулентные бактериофаги развиваются по Литической модели:
- Нуклеиновая кислота фага направляет синтез ферментов фага, используя для этого белоксинтезирующий аппарат бактерии. Фаг тем или иным способом инактивирует ДНК и РНК хозяина, а ферменты фага совсем расщепляют её; РНК фага «подчиняет» себе клеточный аппарат синтеза белка.
- Нуклеиновая кислота фага реплицируется, и направляет синтез новых белков оболочки. Образуются новые частицы фага в результате спонтанной самосборки белковой оболочки (капсид) вокруг фаговой нуклеиновой кислоты; под контролем РНК фага синтезируется лизоцим.
- Лизис клетки: клетка лопается под воздействием лизоцима; высвобождается около 200—1000 новых фагов; фаги инфицируют другие бактерии.
Применение
В медицине
Одной из областей использования бактериофагов является антибактериальная терапия, альтернативная приёму антибиотиков. Например, применяются бактериофаги: стрептококковый, стафилококковый, клебсиеллёзный, дизентерийный поливалентный, пиобактериофаг, коли, протейный и колипротейный и другие.
Бактериофаги применяются также в генной инженерии в качестве векторов, переносящих участки ДНК, возможна также естественная передача генов между бактериями посредством некоторых фагов (трансдукция).
Фаговые векторы обычно создают на базе умеренного бактериофага λ, содержащего двухцепочечную линейную молеклул ДНК. Левое и правое плечи фага имеют все гены, необходимые для литического цикла (репликации, размножения). Средняя часть генома бактериофага λ (содержит гены, контролирующие лизогению, то есть его интеграцию в ДНК бактериальной клетки) не существенна для его размножения и составляет примерно 25 тысяч пар нуклеотидов. Данная часть может быть заменена на чужеродный фрагмент ДНК. Такие модифицированные фаги проходят литический цикл, но лизогения не происходит. Векторы на основе бактериофага λ используют для клонирования фрагментов ДНК эукариот (то есть более крупных генов) размером до 23 т.п.н. Причем, фаги без вставок — менее 38 т.п.н или, напротив, со слишком большими вставками — более 52 т.п.н не развиваются и не поражают бактерии[18].
В биологии
Бактериофаги M13, фаг Т4, T7 и фаг λ используют для изучения белок-белковых, белок-пептидных и ДНК-белковых взаимодействий методом фагового дисплея.
Поскольку размножение бактериофага возможно только в живых клетках бактериофаги могут быть использованы для определения жизнеспособности бактерий. Данное направление имеет большие перспективы, поскольку, одним из основных вопросов при разных биотехнологических процессах является определение жизнеспособности используемых культур. С помощью метода электрооптического анализа клеточных суспензий была показана возможность изучения этапов взаимодействия фаг-микробная клетка[19].
Ссылки
- ↑ Вирусы бактерий
- ↑ Бактериофаг
- ↑ Ackermann H.-W. // Res. Microbiol., 2003. — V. 154. — P. 245—251
- ↑ Hendrix R.W. // Theor. Popul. Biol., 2002. — V. 61. — P. 471—480
- ↑ Suttle C.A. (September 2005), Vuiruses in the sea. Nature 437:356-361.
- ↑ Шестаков С. В. Как происходит и чем лимитируется горизонтальный перенос генов у бактерий. Экологическая генетика 2007. — Т. 5. — № 2. — C. 12-24.
- ↑ 1 2 Tettelin H., Masignani V., Cieslewicz M. J., Donati C., Medini D., Ward N. L., Angiuoli S. V., Crabtree J., Jones A. L., Durkin A. S., Deboy R. T., Davidsen T. M., Mora M., Scarselli M., Margarit y Ros I., Peterson J. D., Hauser C. R., Sundaram J. P., Nelson W. C., Madupu R., Brinkac L. M., Dodson R. J., Rosovitz M. J., Sullivan S. A., Daugherty S. C., Haft D. H., Selengut J., Gwinn M. L., Zhou L., Zafar N., Khouri H., Radune D., Dimitrov G., Watkins K., O’Connor K. J., Smith S., Utterback T. R., White O., Rubens C. E., Grandi G., Madoff L. C., Kasper D. L., Telford J. L.,. Wessels M. R, Rappuoli R., Fraser C. M. Genome analysis of multiple pathogenic isolates of Streptococcus agalactiae: implications for the microbial «pan-genome.» Proc. Natl. Acad. Sci. USA 2005. 102: 13950-13955
- ↑ 1 2 3 4 5 Guttman B., Raya R., Kutter E. Basic Phage Biology, in Bacteriophages: Biology and Applications, (Kutter E. and Sulakvelidze A., ed.), CRP Press, 2005 FL. — Р.29-66.
- ↑ Ковалева Е. Н. Создание биопрепарата на основе выделенных и изученных бактериофагов Enterococcus faecalis: Дис. … канд. биол. наук. — Саратов, 2009. — 151 с
- ↑ Ackermann H.-W. // Res. Microbiol., 2003. — V. 154. — P. 245—251.
- ↑ 1 2 3 4 Ожерельева Н. Г. Краткая Медицинская Энциклопедия, М.: изд-во «Советская Энциклопедия», 1989. — издание второе.
- ↑ Русалеев В. С., Таксономия вирусов бактерий / В. С. Русалеев // Ветеринария. — 1990. — № 12. — C. 25-28.
- ↑ Virus Taxonomy. Classification and Nomenclature of Viruses. Seventh Report of the International Committee on Taxonomy of Viruses / Edited by M.H.V. van Regenmontel et al. — San Diego: Academic Press, 2000. — P. 43-53, 64-129.
- ↑ Raya R.R., Hébert E.M. Isolation of phage via induction of lysogens. Bacteriophages: Methods and Protocols, Volume 1: Isolation, Characterization, and Interaction (Martha R.J. Clokie, Andrew M. Kropinski (eds.), 2009. — V. 501. — P. 23-32.
- ↑ 1 2 Микробиология: учеб. пособие / В. В. Лысак. — Минск : БГУ, 2007. — 430 с.
- ↑ Адамс М., Бактериофаги / М. Адамс. — М.:Медгиз, 1961. — 521 с.
- ↑ Гольдфарб Д. М., Бактериофагия / Д. М. Гольдфарб. — М.: Медгиз, 1961. — 299 с.
- ↑ Щелкунов С. Н. Генетическая инженерия / С. Н. Щелкунов. — Новосибирск : Сиб. унив. изд-во, 2004. — 496 с.
- ↑ Guliy O.I., Bunin V.D., O’Neil D., Ivnitski D., Ignatov O.V. A new electro-optical approach to rapid assay of cell viability // Biosensors and Bioelectronics. 2007. V. 23. P. 583—587.
dic.academic.ru
Фаги - это... Что такое Фаги?
Бактериофа́ги (фаги) (от греч. φάγος — пожирать) — вирусы, избирательно поражающие бактериальные клетки. Чаще всего, бактериофаги размножаются внутри бактерий и вызывают их лизис. Как правило бактериофаг состоит из белковой оболочки и генетического материала -- одноцепочечной или двуцепочечной РНК. Размер частиц приблизительно от 20 до 200 нанометров.
История
Предположение, что бактериофаги имеют корпускулярную природу, было выдвинуто еще Ф. д'Эрелем. Однако, только после изобретения электронного микроскопа удалось увидеть и изучить ультраструктуру фагов. Долгое время представление о морфологии и основные особенности фагов основывались на результатах изучения фагов Т-группы — Т1, Т2,..., Т7, которые размножаются на Е. coli штамма В. Однако, с каждым годом появлялись новые данные касающиеся морфологии и структуры разнообразных фагов, что обусловило необходимость их морфологической классификации.
1 — головка, 2— хвост, 3 — нуклеиновая кислота, 4 — капсид, 5 —"воротничок", 6 — белковый чехол хвоста, 7— фибрилла хвоста, 8 — шипы, 9 — базальная пластинкаЖизненный цикл вирулентных бактериофагов
- Фаг приближается к бактерии, и хвостовые нити связываются с рецепторными участками на поверхности бактериальной клетки.
- Хвостовые нити изгибаются и "заякоривают" шипы и базальную пластинку на поверхности клетки; хвостовой чехол сокращается, заставляя полый стержень входить в клетку; этому способствует фермент лизоцим, который находится в базальной пластинке; таким образом нуклеиновая кислота (ДНК или РНК) вводится внутрь клетки.
- Нуклеиновая кислота фага кодирует синтез ферментов фага, используя для этого белоксинтезирующий аппарат хозяина.
- Фаг тем или иным способом инактивирует ДНК и РНК хозяина, а ферменты фага совсем расщепляют её; РНК фага подчиняет себе клеточный аппарат.
- Нуклеиновая кислота фага реплицируется и кодирует синтез новых белков оболочки.
- Новые частицы фага, образовавшиеся в результате спонтаной самосборки белковой оболочки вокруг фаговой нуклеиновой кислоты; под контролем РНК фага синтезируется лизоцим.
- Лизис клетки: клетка лопается под воздействием лизоцима; высвобождается около 200-1000 новых фагов; фаги инфицируют другие бактерии.
- Стадии 1-7 по времени занимают около 30 минут; этот период называется латентным периодом.
Применение
В медицине
Одной из областей использования бактериофагов является антибактериальная терапия, альтернативная приёму антибиотиков. Например, применяются бактериофаги: стрептококковый, стафилококковый, клебсиеллёзный, дизентерийный поливалентный, пиобактериофаг, коли, протейный и колипротейный и другие.
Бактериофаги применяются также в генной инженерии в качестве векторов, переносящих участки ДНК, возможна также естественная передача генов между бактериями посредством некоторых фагов (трансдукция).
В биологии
Бактериофаги M13, T4, T7 и фаг λ используют для изучения белок-белковых, белок-пептидных и ДНК-белковых взаимодействий методом фагового дисплея.
Ссылки
Wikimedia Foundation. 2010.
dic.academic.ru
Бактериофаги — что это такое?
Заболеваниями верхних дыхательных путей, имеющими бактериальное происхождение, довольно часто страдают люди различных возрастов. Как известно, основное направление в лечении таких состояний занимает антибактериальная терапия.
Особенности
В настоящее время участились случаи, когда прием антибиотиков не проявляет необходимой эффективности, важной для устранения инфекционного агента. Чаще всего это связано с формированием у возбудителя привыкания к определенным видам антибактериальных препаратов. Именно данная ситуация способствовала распространению метода лечения, при котором необходимо использовать препарат Бактериофаг.
Учитывая то, что использование данного метода не получило еще достаточного распространения в наше время, многие люди имеют о нем лишь смутное представление. Разберемся в том, для чего нужны бактериофаги и что это такое в принципе.
Бактериофаги – это вирусные организмы, которые могут существовать лишь внутри бактериальной клетки, оказывая на нее разрушающее воздействие. Эти внутриклеточные паразиты отличаются друг от друга морфологической структурой, а также проявляют избирательность в отношении определенного вида бактериальных клеток. В отличие от клеточных организмов, они содержат только генетический материал, находящийся внутри белковой оболочки.
Обитают данные внутриклеточные паразиты везде, где находятся чувствительные к ним бактериальные клетки.
Им свойственный длительный период существования в любых окружающих средах или организмах, за исключением случаев целенаправленного уничтожающего воздействия. Однако репродукция данных вирусных организмов возможна лишь внутри самой бактерии из-за неимения таких важных клеточных элементов, как рибосомы.
Принцип действия фагов

Изначально бактериофаг прикрепляется к клеточной оболочке бактерии, после чего внедряет свой генетический материал в середину данной клетки. Это существенно влияет на процесс жизнедеятельности бактериального организма, поскольку происходит гибель его собственного гена за счет нарушения всех метаболических процессов.
Главная цель бактериофага заключается в размножении, при этом осуществимо это только при использовании ресурсов бактериальной клетки. По скорости развития процесса различают вирулентные фаги, для них характерно быстрое размножение и гибель бактерии, и умеренные фаги, которые медленно воздействуют на патогенную микрофлору.
Использование бактериофагов
Данное средство терапии инфекционных заболеваний бактериального происхождения с каждым годом набирает все большую популярность по сравнению с антибактериальными препаратами, что в первую очередь обусловлено:
- Отсутствием формирования привыкания к препарату.
- Свободным приемом в комплексе с другими препаратами, в том числе с антибиотиками (по некоторым данным, могут усиливать их действие).
- Отсутствием влияния на собственную микрофлору человека.
- Высокой эффективностью.
- Отсутствием подавляющего действия в отношении иммунитета.
Лечение данными препаратами не имеет противопоказаний, возможно лишь незначительное проявление побочных эффектов, что связано с выделением эндотоксинов из разрушенных бактерий.
В отоларингологии бактериофаги наиболее часто используются при инфекциях верхних дыхательных путей (ангины, ларингиты) и воспалительных процессах в полости носа и уха (гаймориты, отбиты). Обычно их назначают в форме таблеток, растворов для полоскания и орошения, аэрозолей.
Дозировка препаратов варьирует в зависимости от распространенности воспалительного очага и возраста пациента. Средний курс лечения обычно занимает 7–10 дней. Назначает данный метод терапии лечащий врач после установления вида возбудителя, основываясь на результатах проведенных бактериологических исследований.
Виды препаратов

На фармацевтическом рынке уже имеется достаточное количество бактериофагов, которые проявляют активность как по отношению к одному определенному возбудителю, так и к комплексу определенных бактерий. Рассмотрим самые популярные препараты в отоларингологии:
- Секстафаг. Является поливалентным препаратом, активность которого направлена против стрепто- и стафилококков, а также протея, клебсиеллы, синегнойной и кишечной палочки. Выпускается в виде раствора для наружного и внутреннего приема. Часто назначается при гнойно-воспалительных процессах верхних дыхательных путей, полости носа и уха.
- Пиобактериофаг комплексный. Оказывает действие на те же возбудители, что и Секстафаг, дополнительно проявляет активность в отношении энтерококков.
- Пиобактериофаг очищенный. По своему действию аналогичен Секстафагу.
- Стрептококковый фаг. Проявляет свою активность лишь в отношении стрептококка, поэтому применяется при ассоциированных с ним заболеваниях.
- Стафилококковый фаг. Применяется при инфекции, которая вызвана фагочуствительным штаммом стафилококка.
- Синегнойный фаг. Используется для лечения заболеваний, вызванных Pseudomonas aeruginosa.
- Клебсиелл поливалентный. Назначается в случае выявления воспалительных заболеваний со стороны ЛОР-органов, связанных с K.pneumoniae, K.ozaenae, K.rhinoscleromatis.
- Протейный фаг. Применяется в случаях заражения бактериями P.vulgaris, P.mirabilis.
Для всех указанных препаратов характерна высокая эффективность оказываемого действия. Они практически не имеют противопоказаний к назначению, за исключением наличия индивидуальной непереносимости к лекарственному средству. Активно применяются для лечения бактериальных заболеваний у беременных. Детям грудного возраста бактериофаги назначаются в виде клизм или же добавляются в грудное молоко.
Подбирать дозировку и устанавливать срок продолжительности терапии может только лечащий врач. Самостоятельно корректировать лечение запрещено!
elaxsir.ru
Поиск по сайту
Email рассылка
Узнавай первым
об обновлениях на сайте по Email БЕСПЛАТНО! Как только на сайте появятся новые посты, видео или фото, Ты сразу же будешь извещен об этом одним из первых.
Новое на сайте
Новое на форуме
Нет сообщений для показа