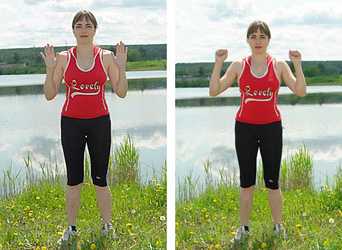Красная кровяная соль — характеристика вещества. Красная соль что это такое
Красная кровяная соль — характеристика вещества
Красная кровяная соль представляет собой кристаллы калия феррицианида. Это вещество синтезируется в искусственных условиях и используется в химической промышленности. Кстати, это вещество известно в мире и под другим названием — гексацианоферрат (III) калия.
Красная кровяная соль и ее свойства
Гексацианоферрат калия представляет собой искусственные кристаллы с моноклинной структурой. Кровяная соль имеет характерный насыщенный красный оттенок, что и отразилось в ее названии.
Кристаллы прозрачные, просвечиваются при наличии света. Интересно, что чем больше кристалл, тем насыщеннее становится цвет. Вещество не окисляется под влиянием воздуха, зато прекрасно растворяется в воде с образованием оранжевого или зелено-желтого раствора. Выветривание калия гексацианоферрата происходит только при нагревании.
При реакции с кислотами образуется токсическое вещество. Именно поэтому красная кровяная соль считается сильным ядом. При попадании в пищеварительную систему вещество вступает в реакцию с желудочными кислотами. Для человека смертельная доза составляет примерно четыре грамма.
Красная кровяная соль и ее применение
Калий гексацианоферрат используют при производстве разного рода электротехники. Кроме того, растворы вещества применяют в процессе проявления фотографий.
Водный раствор этого средства нашел себе применение и в химической промышленности. Здесь его используют как реагент для обнаружения ионов железа.
Кровяная соль употребляется также в пиротехнике. Иногда из нее производят синильную кислоту.
Правила хранения красной кровяной соли
Поскольку данное вещество обладает высокой токсичностью, то и обращаться с ним нужно с особой осторожностью. Кристаллы необходимо предохранять от воздействия кислот, воды и пара. Поскольку при нагревании реагент начинает выветриваться, то нужно предохранять его от воздействия высоких температур. Калий гексацианоферрат следует хранить при температуре не выше сорока градусов по Цельсию.
Не стоит подвергать кристаллы длительному воздействию прямых солнечных лучей. И еще один важный момент: после работы с веществом обязательно следует тщательно вымыть руки.
Желтая кровяная соль и ее свойства
Желтая кровяная соль — это еще одно довольно известное вещество, которое представляет собой желтые прозрачные кристаллы.
Данное вещество известно и под другими названиями, например, гексацианоферат(II) калия, желтое синькали. Интересна история такого тривиального названия, как желтая кровяная соль. Дело в том, что в свое время ее получали путем сплавления с железными опилками и поташом крови и прочих отходов с скотобоен.
Данное вещество постепенно выветривается на воздухе, поэтому кристаллы, как правило, покрывают тонким слоем защитного лака. Вещество хорошо разводится в воде, образуя растворы ярко-желтого цвета. При нагревании начинается процесс выветривания. Как и предыдущий элемент, желтая соль ядовита для человеческого организма, так как быстро взаимодействует с желудочными кислотами, образуя тяжелые токсины.
Поэтому и условия хранения кристаллов сходны — нельзя подвергать их воздействию воды, кислот, влаги, солнечных лучей.
Использование желтой кровяной соли
Данное вещество широко применяют в современной промышленности. Например, из соли изготавливают красящие пигменты. Некоторые производные желтой соли используют в текстильной промышленности в окрашивании тканей, в частности, шелка.
Желтая соль широко применяется в аналитической химии для обнаружения в растворе ионов тех или иных веществ. Например, при реакции соли с ионами трехвалентного железа образуется весьма характерный осадок под названием «берлинская лазурь». При взаимодействии с цинком получается белый осадок соли. А во время реакции с купрумом получается красновато-оранжевый осадок.
fb.ru
Пищевая Гималайская красная соль 482гр
Гималайская красная соль содержит 84 микроэлемента и 200 химических соединений, с повышенным содержанием железа. Геологический возраст более 200 млн. лет
Повсеместно используется как замена поваренной пищевой соли. Такую соль можно встретить на столах европейских ресторанов, и, конечно же, она используется при приготовлении пищи. А также используется при консервировании продуктов, и соления рыбы и мяса.
Добывается Пищевая Гималайская соль исключительно вручную в горах Гималаев.
К лечебным свойствам Пищевой Гималайской соли относятся:
•Очищает организм от шлаков
•Восстанавливает и балансирует водно-солевой обмен
•Стимулирует аппетит
•Способствует регенерации клеток и омоложению всего организма
•Расслабляет мышечные ткани
•Уравновешивает психологическое состояние
•Комплексный терапевтический эффект при использовании в ваннах
•Является источником важных микроэлементов
•Не задерживает воду в тканях, если применяется в нормальных дозах (поваренная соль – задерживает жидкость, даже если применяется в минимальных дозах)
•Имеет слабое слабительное и диуретическое действия
•Улучшает циркуляцию крови и лимфы
•Не растворяется выше нормы, соответственно отсутствует риск отравления при большом потреблении
•Уменьшает похмельный синдром
•Помогает от боли в суставах
Показания к применению пищевой Гималайской соли:
•Расстройства пищеварения
•Ослабление иммунной системы – синдром хронической усталости
•Болезни сердечнососудистой системы
•Болезни мочеполовой системы
•Болезни опорно-двигательного аппарата (заболевания позвоночника, подагра, ревматизм, артроз, артриты и т.д.)
•Болезни полости рта и носоглотки (грипп, пародонтоз, зубная боль, ангины, другие инфекции и т.д.)
•Эндокринные заболевания (тиреотоксикоз, ожирение, мастопатия, женское бесплодие)
•Укусы насекомых – приготовление марлевой повязки с соляным раствором
•Проблемы с метаболизмом
•Нарушения сна
•Болезни кожи (герпес, сыпь, псориаз и т.д. – пораженные части кожи смочить солевым раствором и через несколько минут сполоснуть водой)
•Гипертония
•Отравления
•Водянка
•Астма
Именно поэтому соль называют «квинтэссенцией жизни»
hpcsalt.ru
Красная кровяная соль - это... Что такое Красная кровяная соль?

Гексацианоферрат (III) калия (красная кровяная соль)
Гексацианоферра́т(III) ка́лия (железосинеро́дистый ка́лий, феррициани́д ка́лия, гексацианоферра́т ка́лия) — комплексное соединение трёхвалентного железа K3[Fe(CN)6].
Тривиальные названия
- красная кровяная соль;
- красное синькали.
История и происхождение названия
В 1822 немецким химиком Леопольдом Гмелином соединение было приготовлено путём окисления «жёлтой кровяной соли». Этот факт, а также красный цвет кристаллов, обусловили происхождение названия.
Свойства
Тёмно-красные кристаллы с моноклинной решеткой. Водный раствор зеленовато-жёлтого цвета.
| 0 | 29,9 |
| 10 | 38,3 |
| 20 | 46 |
| 25 | 48,8 |
| 30 | 52,7 |
| 40 | 59,5 |
| 60 | 70,9 |
| 80 | 81,8 |
| 100 | 91,6 |
В этаноле нерастворим.
Гексацианоферрат(III) калия - очень сильный окислитель, особенно в щелочной среде. Окисляет h3S до S, HI до I2, PbO до PbO2, Nh4 до N2 и солей аммония, W до WO42-:
W + 6K3[Fe(CN)6] + 8KOH → 6K4[Fe(CN)6] + K2WO4 + 4h3O
На свету происходит быстрое увеличение значения pH, при помещении в темноту кислотность уменьшается. Это связано со светочуствительностью обратимых реакций:
K3[Fe(CN)6] + h3O ↔ K2[Fe(CN)5Oh3] + KCN
KCN + h3O ↔ HCN + KOH
С солями Fe2+ образует темно-синий осадок турнбулевой сини. Уравнение реакции (в ионной форме):
4Fe2+ + 3[Fe(CN)6]3- → FeIII4[FeII(CN)6]3↓
Ранее считалось, что при этом образуется гексацианоферрат(III) железа(II), то есть FeII3[Fe(CN)6]2, именно такую формулу предлагали для «турнбулевой сини». Теперь известно, что турнбулева синь и берлинская лазурь — одно и то же вещество, а в процессе реакции происходит переход электронов от ионов Fe2+ к гексацианоферрат(III) — иону (валентная перестройка Fe2+ + [Fe3+(CN)6] к Fe3+ + [Fe2+(CN)6] происходит практически мгновенно, обратную реакцию можно осуществить в вакууме при 300°C). Соли Fe3+ при этом не мешают, так как дают только слабое зеленовато-коричневое окрашивание (Гексацианоферрат(III) железа(III) Fe3+[Fe3+(CN)6] устойчив только в растворах).
Эта реакция является аналитической и используется для определения ионов Fe2+.
С концентрированной серной кислотой реагирует, давая FeH(SO4)2, KHSO4, Nh5HSO4 и CO.
С соляной кислотой реагирует давая осадок железосинеродистой кислоты h4[Fe(CN)6].
Реагирует с перекисью бария (эта реакция может использоваться для количестенного определения BaO2):
BaO2 + 2K3[Fe(CN)6] → K6Ba[Fe(CN)6]2 + O2↑
В отличие от гексацианоферрата(II) калия, гексацианоферрат(III) калия ядовит.
Интересно то, что из гексацианоферрата(III) калия можно получить гексацианоферрат(II) калия с помощью перекиси водорода в щелочной среде.
2K3[Fe(CN)6] + h3O2 + 2KOH → 2K4[Fe(CN)6] + 2h3O + O2↑
Дело в том, что в нейтральной среде эта реакция протекает в обратную сторону.
Получение
Получают калия гексацианоферрат(III) окислением K4[Fe(CN)6] хлором в солянокислой среде, бромом или другим сильным окислителем, например, перманганатом калия.
Применение
Компонент тонирующих, отбеливающих, усиливающих, ослабляющих растворов в фотографии, электролит в хемотронных приборах, компонент электролитов в гальванопластике, реагент для обнаружения Fe2+ (см. выше), Li+ Sn2+, а также в качестве сильного окислителя.
В почвоведении используют для качественного определения оглеения (солей двухвалентного железа). Химическая реация описана выше.
Мнемонические правила
Для того, чтобы запомнить формулу красной кровяной соли K3[Fe(CN)6] и не перепутать ее с формулой желтой кровяной соли K4[Fe(CN)6], существует несколько мнемонических правил:
- В соли красной кровяной калий с тройкой за стеной. Дальше - феррум, шесть цианов: все готово без обманов.
- Число атомов калия соответствует числу букв в английских названиях солей: "gold" - 4 буквы, то есть 4 атома калия - желтая кровяная соль K4[Fe(CN)6]. "Red" - три буквы, то есть три атома калия - красная кровяная соль - K3[Fe(CN)6].
См. также
Wikimedia Foundation. 2010.
dic.academic.ru
Красная кровяная соль — характеристика вещества
Красноватая кровяная соль представляет собой кристаллы калия феррицианида. Это вещество синтезируется в искусственных критериях и употребляется в хим индустрии. Кстати, это вещество понятно в мире и под другим заглавием — гексацианоферрат (III) калия.
Красноватая кровяная соль и ее характеристики
Гексацианоферрат калия представляет собой искусственные кристаллы с моноклинной структурой. Кровяная соль имеет соответствующий насыщенный красноватый колер, что и отразилось в ее заглавии.
Кристаллы прозрачные, просвечиваются при наличии света. Любопытно, что чем больше кристалл, тем насыщеннее становится цвет. Вещество не окисляется под воздействием воздуха, зато отлично растворяется в воде с образованием оранжевого либо зелено-желтого раствора. Выветривание калия гексацианоферрата происходит только при нагревании.
При реакции с кислотами появляется токсическое вещество. Вот поэтому красноватая кровяная соль считается сильным ядом. При попадании в пищеварительную систему вещество вступает в реакцию с желудочными кислотами. Для человека смертельная доза составляет приблизительно четыре грамма.
Красноватая кровяная соль и ее применение
Калий гексацианоферрат употребляют при производстве различного рода электротехники. Не считая того, смеси вещества используют в процессе проявления фото.
Аква раствор этого средства отыскал для себя применение и в хим индустрии. Тут его употребляют как реагент для обнаружения ионов железа.
Кровяная соль употребляется также в пиротехнике. Время от времени из нее создают синильную кислоту.
Правила хранения красноватой кровяной соли
Так как данное вещество обладает высочайшей токсичностью, то и обращаться с ним необходимо с особенной осторожностью. Кристаллы нужно защищать от воздействия кислот, воды и пара. Так как при нагревании реагент начинает выветриваться, то необходимо защищать его от воздействия больших температур. Калий гексацианоферрат следует хранить при температуре не выше сорока градусов по Цельсию.
Не стоит подвергать кристаллы долговременному воздействию прямых солнечных лучей. И очередной принципиальный момент: после работы с веществом непременно следует кропотливо вымыть руки.
Желтоватая кровяная соль и ее характеристики
Желтоватая кровяная соль — это очередное достаточно известное вещество, которое представляет собой желтоватые прозрачные кристаллы.
Данное вещество понятно и под другими наименованиями, к примеру, гексацианоферат(II) калия, желтоватое синькали. Увлекательна история такового очевидного наименования, как желтоватая кровяная соль. Дело в том, что в свое время ее получали методом сплавления с стальными опилками и поташом крови и иных отходов с скотобоен.
Данное вещество равномерно выветривается на воздухе, потому кристаллы, обычно, покрывают узким слоем защитного лака. Вещество отлично разводится в воде, образуя смеси ярко-желтого цвета. При нагревании начинается процесс выветривания. Как и предшествующий элемент, желтоватая соль ядовита для организма человека, потому что стремительно ведет взаимодействие с желудочными кислотами, образуя томные токсины.
Потому и условия хранения кристаллов сходны — нельзя подвергать их воздействию воды, кислот, воды, солнечных лучей.
Внедрение желтоватой кровяной соли
Данное вещество обширно используют в современной индустрии. К примеру, из соли изготавливают красящие пигменты. Некие производные желтоватой соли употребляют в текстильной индустрии в окрашивании тканей, а именно, шелка.
Желтоватая соль обширно применяется в аналитической химии для обнаружения в растворе ионов тех либо других веществ. К примеру, при реакции соли с ионами трехвалентного железа появляется очень соответствующий осадок под заглавием «берлинская лазурь». При содействии с цинком выходит белоснежный осадок соли. А во время реакции с купрумом выходит красновато-оранжевый осадок.
Что такое розовая Гималайская соль
Красная (розовая) Гималайская соль считается самой полезной. Она не только не вредит организму, но и обладает массой полезных и даже лечебных свойств. Эта соль содержит 84 минерала и микроэлемента, которые необходимы для организма.

Считается, что единственная гарантия качества и полезности – покупка соли из стран ее добычи: Индия, Непал, Пакистан.
Но не менее полезна, хотя гораздо менее разрекламирована, красная крымская соль, добываемая из соленых озер Сасык-Сиваш, Мойнаки и залива Сиваш, расположенных на севере Крыма. Эти поля были почти заброшены, сейчас появляются идеи восстановить производство.
Наибольшие объемы добычи этой соли были зафиксированы в конце 19-го века, когда крымские солевары продавали более 75 тысяч тонн соли.
Историки уверяют: освоение крымских соляных озер было начато еще половцами. Или скифами, что еще намного интереснее!)).
Розовый (красный) цвет соль получает из-за высокого содержания природного бета-каротина.
В соляных озерах Крыма - существует редкий феномен. Морская вода, отведенная в садочные бассейны, по мере выпаривания приобретает совершенно марсианский кирпично-красный цвет.
Над этой загадкой бились еще античные ученые. Но разгадать ее удалось лишь в 1903 году. Оказалось, что только в этих районах в морской воде живет микроводоросль Dunaliella Salina. Она сумела приспособиться к жестким условиям ультрасоленой воды и солнечной радиации, научившись вырабатывать бета-каротин. Это волшебное вещество помогает выжить не только водоросли, но и человеку, повышает иммунитет, помогает организму приспособиться к неблагоприятным условиям, при этом не вызывает аллергии и не имеет побочных эффектов и противопоказаний.
Именно благодаря микроводоросли и ее бета-каротину рассол приобретает этот марсианский вид. Когда вода полностью испаряется, весь бета-каротин вместе с морским йодом, магнием и бромом включается в структуру растущих соляных кристаллов. Отличить такую соль от обычной просто. Соль с бета-каротином – розовая.
Если растворить такую соль в воде и потом снова выпарить, получается обычная белая соль. Йод, магний и бета-каротин уйдут в воду. Чтобы уберечь драгоценные микроэлементы, соль не подвергают термической обработке и не размалывают заранее. Ее мелят маленькими порциями в ручной мельнице прямо в тарелку.
В период бурного цветения водорослей, морские озера насыщаются множеством биоактивных веществ (т.к. b-каротин, природный воск, эфирные масла, йод), приобретая ярко-малиновый цвет, а добываемая соль включает биокомпоненты в свою кристаллическую решетку. Основное отличие от солей древних морей (каменной соли) - кратчайший срок от производства до применения, сохранение (помимо химического состава) живой биологии моря.
Как отличить по внешнему виду: крупный, неправильной формы кристалл, с розовым оттенком. Повторить форму и цвет кристалла искусственно невозможно.
Собирается вручную, 1 раз в год (сентябрь-октябрь) в экологически чистой прибрежной зоне, с использованием древних методов естественного гелеоупаривания.
Причем настоящая «розовая вода» встречается лишь в четырех местах земного шара. Одно из этих мест — в Крыму: соленое озеро Сасык-Сиваш недалеко от города Саки.
www.pravilnoe-pokhudenie.ru
Поделитесь ссылкой c друзьями
|
Другие записи в блокноте:Что делать с пылью?Что вы знаете о сне?Как заставить себя заниматься спортом?Как правильно закаляться?Как похудеть с удовольствием?Что полезного в яблоках?Что может вылечить еда?Как вспомнить все?Как необычно провести отпуск?Как повысить иммунитет? |
|
www.chasyogi.ru
ЖЕЛТАЯ КРОВЯНАЯ СОЛЬ ФОРМУЛА - О некоторых комплексных солях железа
 Эти же концентрации желтой кровяной соли не влияют на величину растворенного в воде кислорода. Берлинскую лазурь можно получить, добавляя к растворам гексацианоферрата (II) калия («жёлтой кровяной соли») соли трёхвалентного железа. Ещё один способ состоит в добавлении к растворам гексацианоферрата (III) калия («красной кровяной соли») солей двухвалентного железа.
Эти же концентрации желтой кровяной соли не влияют на величину растворенного в воде кислорода. Берлинскую лазурь можно получить, добавляя к растворам гексацианоферрата (II) калия («жёлтой кровяной соли») соли трёхвалентного железа. Ещё один способ состоит в добавлении к растворам гексацианоферрата (III) калия («красной кровяной соли») солей двухвалентного железа.
Это, а также жёлтый цвет кристаллов, обусловили название соединения. При этом получалось соединение, очень похожее на «берлинскую лазурь», такого же красивого синего цвета, также существующего в растворимой и нерастворимой формах.
Получающийся гексацианоферрат(II) калия-железа(III) растворим, поэтому носит название «растворимая берлинская лазурь». Ионыжелеза (III) в растворе можно определить с помощью качественных реакций. Если в растворе есть ионы железа (III), образуется гидроксид железа (III) Fe(OH)3.
В присутствии иона железа (III) при добавлении роданида калия образуется вещество красного цвета. Это ‑ роданид железа (III). Роданид от греческого «родеос» — красный. Дисбах купил у торговца необычный поташ (карбонат калия): раствор этого поташа при добавлении солей железа получался синим. При проверке поташа оказалось, что он был прокаленс бычьей кровью. Выщелачиванием такого сплава получали желтую кровяную соль. Сейчас берлинскую лазурь используют для получения печатной краски и подкрашивания полимеров.
Этот способ по сравнению с вышеописанным имеет двоякую выгоду: весь цианид получается в соединении и нет цианокислых солей, как при накаливании с поташем. В промышленности калий железистосинеродистый применяют для производства красок, красной кровяной соли, синильной кислоты и других веществ, для цементации сталей и т.д.
Если к раствору хлорного железа, который подкислен небольшим количеством соляной кислоты, прилить немного раствора железистосинеродистого калия, то получится тёмно-синий осадок берлинской лазури. Реакция образования берлинской лазури широко используется в аналитической химии для открытия ионов железа. Соли Fe3+ при этом не мешают, так как дают только слабое зеленовато-коричневое окрашивание (Гексацианоферрат(III) железа(III) Fe3+ устойчив только в растворах).
В помощь молодому учителю
С ионом железа Fe3+ комплексный ион образует нерастворимую соль интенсивного синего цвета , известную под несколькими названиями. Красная кровяная соль была получена в 1822 г. выдающимся немецким химиком-аналитиком Леопольдом Гмелиным.
В настоящее время считают, что состав красной кровяной соли отвечает формуле К3 и согласно номенклатуре называется гексацианоферратом(III) калия**. Комплексный ион этой соли менее устойчив, чем желтой кровяной соли, и распадается с выделением иона СN–. По этой причине красная кровяная соль представляет собой сильное ядовитое вещество. Методом приготовления перенасыщенного раствора жёлтой кровяной соли при температуре 60-70 градусов и дальнейшим остывании данного раствора.

Кристаллы легко растворимы в воде, имеют яркий жёлтый цвет, при нагревании обезвоживаются, при реакции с кислотами ядовиты, оставляют синие пятна (синькали/синильная кислота). Данные бактериологического анализа показали, что концентрации желтой кровяной соли до 25 мг / л не задерживают развития бактерий, участвующих в процессах минерализации органических веществ.
СПОСОБ СИНТЕЗА (искусственного выделения)
Полутвердую реакционную смесь оставляют стоять на несколько часов, после чего е разлагают кипящей водой. Полученную смесь фильтруют; по охлаждении выделяются с хорошим выходом кристаллы альдегида.

При этом важно избегать введения избытка желтой кровяной соли, в присутствии которого не образуется осадок берлинской лазури
Для удаления железа желтую кровяную соль, взятую из расчета 5 6 г на 1 г железа в электролите, растворяют в малом объеме воды и при перемешивании вливают в электролит небольшими порциями. Чтобы в ферроцианиде калия открыть аналитически железо, необходимо разрушить комплекс ( стр. Это производят путем выпаривания с концентрированной серной кислотой.
В некоторых источниках его называют Иоганном Якобом Дизбахом (нем.Johann Jacob Diesbach). Интенсивный ярко-синий цвет соединения и место получения дали начало названию. Название «турнбулева синь» происходит от названия шотландской фирмы «Артур и Турнбуль», которая в конце восемнадцатого века производила краски.

Железная лазурь в воде не растворима, неядовита, обладает высокой красящей способностью, светостойкостью и атмосферостойкостью. Железная лазурь, благодаря хорошей укрывистости и красивому синему цвету находит широкое применение в качестве пигмента для изготовления красок и эмалей. Также её применяют в производстве печатных красок, синей копирки, подкрашивания бесцветных полимеров типа полиэтилена. Применение железной лазури ограничено её неустойчивостью по отношению к щелочам, под действием которых разлагается с выделением гидроксида железа Fe(OH)3.
В таких материалах в качестве синего пигмента, как правило используют органический пигмент голубой фталоцианиновый. В смеси с маслянистыми материалами используется для контроля плотности прилегания поверхностей и качества их обработки. В XIX веке использовалась в России и Китае для подкрашивания спитой заварки, а также для перекраски чёрного чая в зелёный. Чай и чайная торговля в России и других государствах: Производство, потребление и распределение чая». — Издание А. Г. Кузнецова.
Основание нерастворимо в воде и бурого цвета. (Гидроксид железа (II) Fe(OH)2. Берлинская лазурь была получена случайно в начале 18 века в Берлине красильных дел мастером Дисбахом.
В их синтезе к «красной кровяной соли» добавляли соль железа (II) (железный купорос). Если смешать раствор желтой кровяной соли с раствором соли железа ( Ш), то получается темно-синий осадок — берлинская лазурь. Среди комплексных соединений железа встречаются два очень сходных по названию и близких по составу: желтая кровяная соль K4 и красная кровяная соль К3*. Для того, чтобы избежать соединения углерода с железом при плавлении прибавляют поташ: примерно 8 частей жёлтой кровяной соли и 3 части поташа.
mariantas.ru
Поиск по сайту
Email рассылка
Узнавай первым
об обновлениях на сайте по Email БЕСПЛАТНО! Как только на сайте появятся новые посты, видео или фото, Ты сразу же будешь извещен об этом одним из первых.
Новое на сайте
Новое на форуме
Нет сообщений для показа